��Ŀ����
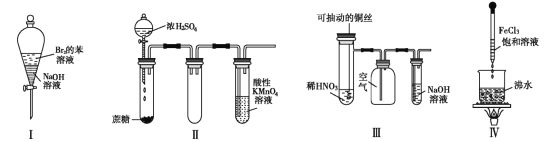
����Ŀ����ͼ������ˮ������Ӧ��ʵ��װ�á���Ӳ�ʲ������з��뻹ԭ���ۺ�ʯ����(ʯ���������²��ϣ���ˮ��������Ӧ)�Ļ������ȣ���ͨ��ˮ�������Ϳ�����ɸ���������ˮ������Ӧ��ʵ�顣
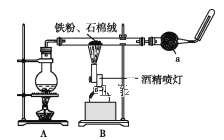

��1����֪��ʵ�鷴Ӧ�ķ�Ӧ����ʽΪ��__Fe+__H2O![]() __Fe3O4+__H2������ƽ����
__Fe3O4+__H2������ƽ����
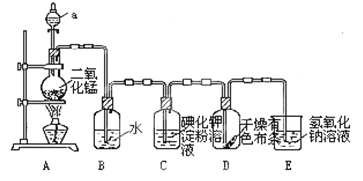
��2������a��������___��
��3��ijͬѧΪ���о�һ��ʱ�������۵�ת���ʣ����������ʵ�飺ȷ����һ�����������۽��з�Ӧ��������Ӧ�����������������������۵�ת���ʡ�
�ٸ�ͬѧӦ���ȵ�ȼ__(�A����B��)���ľƾ���(��ƾ����)�������������������ѡ��ͼ��__(��ס����ҡ�����)װ�á�
�ڳ�ȡ5.6g����������ʯ����ϣ�Ȼ����ȷ�Ӧһ��ʱ�䡣���������������ڱ�״����Ϊ0.448L�������۵�ת����Ϊ___����ת����=![]() ��
��
��4����Ӳ�ʲ������з�Ӧ��Ĺ�������ȫ��ȡ�������ձ��У����������������ܽⲢ���ˣ�Ϊ̽����Ӧ����Һ�п��ܵ������ӣ�С��ͬѧ��������ʵ�飬���㽫�±�����������
���� | ���� | ����(�����ӷ���ʽ��ʾ) | ���� |
��.ȡ�����μ�KSCN��Һ | ��Һ�����ɫ | ��Fe3O4+8H+=Fe2++2Fe3++4H2O ��___ | ��.��Ӧ�����Һ��������___ |
��.ȡ�����μ�NaOH��Һ | �տ�ʼ����������һ��ʱ����ȳ��ְ�ɫ������Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ___ɫ | ��___ ��Fe2++2OH��=Fe(OH)2�� ��4Fe(OH)2+2H2O+O2=4Fe(OH)3 |
���𰸡�3 4 1 4 ����� A �� 15% Fe+2Fe3+��3Fe2+ ��� OH��+H+��H2O H����Fe2��
��������
��1�����ݻ��ϼ���������ƽ��
��2������װ���ص��жϣ�
��3���ٻ�ԭ��������ˮ������Ӧ����Ӧ�ȵ�ȼA���ƾ��ƣ�
�ڸ��ݷ���ʽ���㣻
��4�����۹������ܽ�������ӷ�Ӧ�����������ӡ�
��1��Fe��ˮ������Ӧ��Fe�Ļ��ϼ���0�۱�Ϊ+8/3�ۣ�H�Ļ��ϼ���+1�۱�Ϊ0�ۣ���С������Ϊ8����Fe��ϵ��Ϊ3��ˮ��ϵ��Ϊ4��������ϵ��Ϊ4����ʽΪ3Fe+4H2O![]() 1Fe3O4+4H2��
1Fe3O4+4H2��
��2������װ��ͼ����֪����aΪ����ܣ�
��3����Ϊ��ʹ��ԭ��������ˮ������Ӧ����Ӧ�ȵ�ȼA���ƾ���ʹ����װ�ó���ˮ�������ٵ�ȼB���ƾ��ƣ�װ�ü����ռ����壻
���ڱ�������������Ϊ0.448L����0.02mol�����ݷ���ʽ����0.02mol��������μӷ�Ӧ������Ϊ0.015mol������Ϊ0.84g�����۵�ת����=0.84/5.6��100%=15%��
��4����.�������۹����������������������۷�Ӧ�����������ӣ����ӷ���ʽΪFe+2Fe3+��3Fe2+����Һ���������ӣ���μ�KSCN��Һ�����ɫ��
��.�ܽ����ʱ���������������NaOH��Һʱ�����������ӷ�Ӧ����ˮ�����ӷ���ʽΪOH��+H+��H2O�������������ӷ�Ӧ����������������������������������������Ӧ������������������Ϊ�����ɰ�ɫ������Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ��
��.�������������Һ�е����������������ӡ������ӡ�

����Ŀ����һ��������ܱ������У��������»�ѧ��Ӧ��N2(g)+3H2(g)![]() 2NH3(g) ��H��0���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±�������������⡣
2NH3(g) ��H��0���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±�������������⡣
t/�� | 25 | 125 | 225 | �� |
K | 4.1��105 | K1 | K2 | �� |
��1���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK=________��K1______K2����������������������������������ѹǿʹƽ��������Ӧ�����ƶ�����ƽ�ⳣ��_________������������������������
��2���жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������____________������ţ���
A��2��H2������= 3��NH3���棩 B�����������ܶȱ��ֲ���
C��������ѹǿ���ֲ��� D��N2���������ʵ���H2����������
E�������������ƽ����Է�����������ʱ����仯 F������������ɫ���ֲ���
��3������ͬ����N2��H2�ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������У�����������Ӧ�õ������������ݣ�
ʵ���� | �¶ȣ��棩 | ��ʼ����mol�� | ƽ������mol�� | �ﵽƽ������ʱ�䣨min�� | |
N2 | H2 | NH3 | |||
1 | 650 | 2 | 4 | 0.9 | 9 |
2 | 900 | 1 | 2 | 0.3 | 0.01 |
ʵ��1������(NH3)��ʾ�ķ�Ӧ����Ϊ______��ʵ��2�����ʱ�ʵ��1���ԭ����____________��
��4��������Ʋ��ø��������ӵ������SCY�մɣ��ܴ���H+����ʵ���˳�ѹ�¼��ܺϳɰ����ܷ����ʵ��װ�ã���ͼ�������������ĵ缫��ӦΪ_____________��