题目内容
【题目】某研究性学习小组为了探究醋酸的电离情况,进行了如下实验。
探究浓度对醋酸电离程度的影响
用pH计测定25 ℃时不同浓度的醋酸的pH,其结果如下:
醋酸浓度/(mol/L) | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
回答下列问题:
(1)写出醋酸的电离方程式:___________________________________________。
(2)醋酸溶液中存在的微粒有________________________________________。
(3)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是________________________________________________________________________。
(4)从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度将(填“增大”、“减小”或“不变”)__________。
【答案】(1)CH3COOH![]() CH3COO-+H+
CH3COO-+H+
(2)H+;CH3COO-;CH3COOH;OH-
(3)合理答案均可得分
(4)增大
【解析】
试题分析:(1)醋酸是弱电解质,在水溶液里部分电离生成醋酸根离子和氢离子,电离方程式为:CH3COOH![]() CH3COO-+H+。
CH3COO-+H+。
故答案为:CH3COOH![]() CH3COO-+H+;
CH3COO-+H+;
(2)醋酸的电离方程式为CH3COOHCH3COO-+H+,则溶液中存在的微粒有:H2O、
CH3COOH、CH3COO-、H+、OH-。
故答案为:H2O、CH3COOH、CH3COO-、H+、OH-;
(3)当醋酸浓度为0.001mol/L 时,溶液中的氢离子浓度小于0.001mol/L,说明醋酸部
分电离为弱电解质。
故答案为:当醋酸浓度为0.001mol/L 时,溶液中的氢离子浓度小于0.001mol/L;
(4)根据表中数据知,醋酸为0.0100mol/L,溶液的pH3.38,醋酸为0.0010mol/L,溶液的pH为3.88,所以醋酸浓度越小,醋酸的电离程度增大。
故答案为:增大。

 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案【题目】氯仿(CHCl3)常用作有机溶剂和麻醉剂,常温下在空气中易被氧化。实验室中可用热还原CCl4法制备氯仿,装置示意图及有关数据如下:
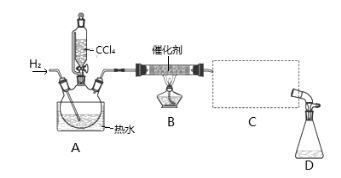
物质 | 相对分子质量 | 密度/(g·mL-1) | 沸点/℃ | 水中溶解性 |
CHCl3 | 119.5 | 1.50 | 61.3 | 难溶 |
CCl4 | 154 | 1.59 | 76.7 | 难溶 |
实验步骤:
①检验装置气密性;②开始通入H2; ③点燃B处酒精灯;
④向A处水槽中加入热水,接通C处冷凝装置的冷水; ⑤向三颈瓶中滴入20 mLCCl4;
⑥反应结束后,停止加热,将D处锥形瓶中收集到的液体分别用适量NaHCO3溶液和水洗涤,分出的产物加入少量无水CaCl2固体,静置后过滤;
⑦对滤液进行蒸馏纯化,得到氯仿15 g。请回答:
(1)若步骤②和步骤③的顺序颠倒,则实验中产生的不良后果可能为 。
(2)B处中发生主要反应的化学方程式为 。
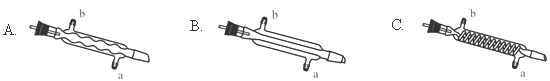
(3)C处中应选用的冷凝管为 (填选项字母);冷水应从该冷凝管的 (填“a”或“b”)口接入。
(4)步骤⑥中,用水洗涤的目的为 。
(5)该实验中,氯仿的产率为 。
(6)氯仿在空气中能被氧气氧化生成HCl和光气(COCl2),该反应的化学方程式为 。
