题目内容
12.对室温下pH相同、体积相同的氨水和氢氧化钠溶液分别采取下列措施,其中叙述正确的是( )| A. | 分别加水稀释10倍,两溶液的pH仍相等 | |
| B. | 温度升高10℃,两溶液的pH均不变 | |
| C. | 加入适量的氯化铵晶体后,两溶液的pH均减小 | |
| D. | 用相同浓度的盐酸中和至反应完全时,消耗盐酸的体积相同 |
分析 NaOH是强碱,一水合氨是弱碱,室温下,pH相等氨水和NaOH溶液中,氨水浓度大于NaOH,
A、加水稀释促进一水合氨电离;
B、升高温度,一水合氨电离程度增大;
C、加入适量的氯化铵晶体,抑制一水合氨电离,NaOH和氯化铵反应生成氯化钠和一水合氨;
D、用HCl中和,消耗盐酸的体积与碱的物质的量成正比.
解答 解:NaOH是强碱,一水合氨是弱碱,室温下,pH相等氨水和NaOH溶液中,氨水浓度大于NaOH,
A、加水稀释促进一水合氨电离,则稀释后氨水的pH大于氢氧化钠,故A错误;
B、升高温度,一水合氨电离程度增大,所以氨水的pH增大,故B错误;
C、加入适量的氯化铵晶体,抑制一水合氨电离,NaOH和氯化铵反应生成氯化钠和一水合氨,所以加入适量的氯化铵晶体后,两溶液的pH均碱小,故C正确;
D、用HCl中和,消耗盐酸的体积与碱的物质的量成正比,pH相等、体积相等的氨水和氢氧化钠溶液,一水合氨的物质的量大于氢氧化钠,所以氢氧化钠消耗的盐酸少,故D错误;
故选C.
点评 本题考查了弱电解质的电离,明确弱电解质的电离特点是解本题关键,易错选项是D,注意消耗酸的物质的量与碱的物质的量成正比,与电解质强弱无关,为易错点.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案
相关题目
20.无水AlCl3是一种重要的化工原料.某课外探究小组尝试制取无水AlCl3,查阅资料获得下列信息:无水AlCl3在178℃升华,极易潮解,遇到水蒸气会产生白色烟雾.
探究一 无水AlCl3的实验室制备
利用下图装置,用干燥、纯净的氯气在加热条件下与铝粉(已除去氧化膜)反应制取无水AlCl3.供选择的药品:①铝粉 ②浓硫酸 ③稀盐酸 ④饱和食盐水 ⑤二氧化锰粉末 ⑥无水氯化钙 ⑦稀硫酸 ⑧浓盐酸 ⑨氢氧化钠溶液

(1)写出装置A烧瓶中发生的反应方程式MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(2)实验开始前,先检查装置气密性,然后装入药品,接下来的步骤依次是bca(填序号)
a.加热D中硬质玻璃管
b.往A烧瓶中加入液体
c.点燃A中的酒精灯
(3)上述供选药品中本实验无需用到的是③⑦(填数字序号).
(4)写出无水AlCl3与水蒸气反应的化学方程式AlCl3+3H2O(g)=Al(OH)3+3HCl.
探究二 无水AlCl3的含量测定及结果分析
取D中反应后所得固体2.0g,与足量氢氧化钠溶液反应,测定生成气体的体积(体积均换算成标准状况),重复测定三次,数据如下:
(5)根据表中数据,计算所得固体中无水AlCl3的质量分数86.5%;.
(6)有同学认为测得的无水AlCl3的质量分数偏低,你认为可能的原因有①②:
①制备的氯气不足 ②固体和气体无法充分接触 ③无水AlCl3发生升华,造成损失
探究三 离子浓度对氯气制备的影响
二氧化锰粉末和浓盐酸的反应随着盐酸的浓度降低,反应停止不再产生氯气.探究小组对盐酸浓度降低影响氯气生成的原因进行如下探究:
(7)提出假设 假设1:Cl-浓度降低影响氯气的生成
假设2:H+浓度降低影响氯气的生成.
(8)设计方案进行实验.限选试剂:浓H2SO4、NaCl固体、MnO2固体、稀盐酸.
探究一 无水AlCl3的实验室制备
利用下图装置,用干燥、纯净的氯气在加热条件下与铝粉(已除去氧化膜)反应制取无水AlCl3.供选择的药品:①铝粉 ②浓硫酸 ③稀盐酸 ④饱和食盐水 ⑤二氧化锰粉末 ⑥无水氯化钙 ⑦稀硫酸 ⑧浓盐酸 ⑨氢氧化钠溶液

(1)写出装置A烧瓶中发生的反应方程式MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(2)实验开始前,先检查装置气密性,然后装入药品,接下来的步骤依次是bca(填序号)
a.加热D中硬质玻璃管
b.往A烧瓶中加入液体
c.点燃A中的酒精灯
(3)上述供选药品中本实验无需用到的是③⑦(填数字序号).
(4)写出无水AlCl3与水蒸气反应的化学方程式AlCl3+3H2O(g)=Al(OH)3+3HCl.
探究二 无水AlCl3的含量测定及结果分析
取D中反应后所得固体2.0g,与足量氢氧化钠溶液反应,测定生成气体的体积(体积均换算成标准状况),重复测定三次,数据如下:
| 第一次实验 | 第二次实验 | 第三次实验 | |
| D中固体用量 | 2.0g | 2.0g | 2.0g |
| 氢气的体积 | 334.5mL | 336.0mL | 337.5mL |
(6)有同学认为测得的无水AlCl3的质量分数偏低,你认为可能的原因有①②:
①制备的氯气不足 ②固体和气体无法充分接触 ③无水AlCl3发生升华,造成损失
探究三 离子浓度对氯气制备的影响
二氧化锰粉末和浓盐酸的反应随着盐酸的浓度降低,反应停止不再产生氯气.探究小组对盐酸浓度降低影响氯气生成的原因进行如下探究:
(7)提出假设 假设1:Cl-浓度降低影响氯气的生成
假设2:H+浓度降低影响氯气的生成.
(8)设计方案进行实验.限选试剂:浓H2SO4、NaCl固体、MnO2固体、稀盐酸.
| 步骤 | 实验操作 | 预测现象和结论 |
| ① | 往不再产生氯气的装置中,加入NaCl固体,继续加热 | 若有黄绿色气体生成,则假设1成立 |
| ② | 往不再产生氯气的装置中,加入浓硫酸并继续加热 | 若有黄绿色气体生成,则假设2成立 |
7.已知0.1mol/L乙二酸溶液的pH大于1,取等体积的乙二酸溶液与NaOH溶液混合,测得溶液的pH=7,则乙二酸与NaOH物质的量浓度的比值( )
| A. | 小于$\frac{1}{2}$ | B. | 大于$\frac{1}{2}$,小于1 | C. | 等于$\frac{1}{2}$ | D. | 大于1,小于2 |
17. 已知25℃时部分弱电解质的电离平衡常数数据如下表:
已知25℃时部分弱电解质的电离平衡常数数据如下表:
回答下列问题:
(1)物质的量浓度均为0.1mol•L一1的四种溶液:a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3,pH由小到大的排列顺序是adcb(用字母表示)
(2)常温下,0.1mol•L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是BD(填序号)
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(3)体积均为l00mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数<(填“>”、“<”或“=”)CH3COOH的电离平衡常数.
(4)25℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中:
①c(CH3COO-)-c(Na+)=9.9×10-7mol•L-1(填精确值)
②$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$=18.
 已知25℃时部分弱电解质的电离平衡常数数据如下表:
已知25℃时部分弱电解质的电离平衡常数数据如下表:| 化学式 | CH3COOH | H2CO3 | HClO | |
| 平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
(1)物质的量浓度均为0.1mol•L一1的四种溶液:a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3,pH由小到大的排列顺序是adcb(用字母表示)
(2)常温下,0.1mol•L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是BD(填序号)
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(3)体积均为l00mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数<(填“>”、“<”或“=”)CH3COOH的电离平衡常数.
(4)25℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中:
①c(CH3COO-)-c(Na+)=9.9×10-7mol•L-1(填精确值)
②$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$=18.
4.制取无水酒精时,通常需向工业酒精中加入下列物质,并加热蒸馏,该物质是( )
| A. | 无水硫酸铜 | B. | 浓硫酸 | C. | 新制的生石灰 | D. | 氢氧化钙 |
1.下列说法正确的是( )
| A. | 二氧化硅的结构式:O=Si=O | |
| B. | H2O沸点高于NH3,是因为H2O分子间存在氢键而NH3分子间不存在氢键 | |
| C. | 含有金属离子的晶体一定是离子晶体 | |
| D. | 分子晶体中一定存在分子间作用力,不一定存在共价键 |

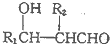 (R1、R2为烃基或H)
(R1、R2为烃基或H)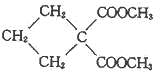 +HBr+HCl
+HBr+HCl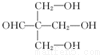 .
. .
.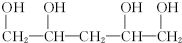 .
. .
.