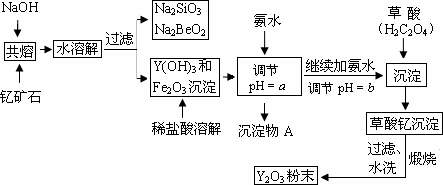
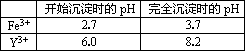
题目内容
|
在10 mL 0.1 mol·L-1 H2SO4溶液中逐滴加入0.1 mol·L-1 Ba(OH)2溶液至过量,溶液的导电能力将 | |
| [ ] | |
A. |
逐渐减小 |
B. |
逐渐增大 |
C. |
不变 |
D. |
先减小后增大 |
答案:D
解析:
解析:
因为加入氢氧化钡会与硫酸发生反应,造成溶液中离子浓度减小,导电能力减弱,随着氢氧化钡继续滴加,溶液中离子浓度会增加,导电能力将增强.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
|
下列离子方程式正确的是 | |
| [ ] | |
A. |
氯化铵溶液呈酸性 NH |
B. |
氢硫酸电离 H2S |
C. |
向小苏打溶液中加入醋酸溶液 HCO |
D. |
在标准状况下,向10 mL 0.1 mol·L-1 FeBr2溶液中通入22.4 mL Cl2 2Fe2++2Br-+2Cl2 |
|
在相同的温度时100 mL 0.01 mol·L-1的醋酸溶液与10 mL 0.1 mol·L-1醋酸溶液相比较,下列数值前者大于后者的是 | |
| [ ] | |
A. |
中和时所需氢氧化钠的物质的量 |
B. |
H+浓度 |
C. |
H+的物质的量 |
D. |
CH3COOH的物质的量 |
 NH3+H+
NH3+H+ 2H++S2-
2H++S2- CO2+H2O
CO2+H2O 2Fe3++Br2+4Cl-
2Fe3++Br2+4Cl-