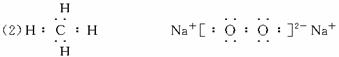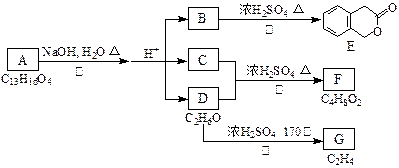题目内容
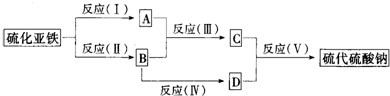
(14分)下图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物。

已知:
①反应 能放出大量的热,该反应曾应用于铁轨的焊接;
能放出大量的热,该反应曾应用于铁轨的焊接;
②I是一种常见的温室气体,它和 可以发生反应:2E+I
可以发生反应:2E+I 2F+D,F中的E元素的质量分数为60%.
2F+D,F中的E元素的质量分数为60%.
回答问题:
(1)①中反应的化学方程式为________________________________;
(2)化合物Ⅰ的电子式为______________________,它的空间构型是_________;
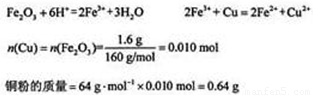
(3)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需铜粉的质量______________________;
(4)C与过量NaOH溶液反应的离子方程式为_______________________,反应后溶液与过量化合物Ⅰ反应的离子方程式为_______________________;
(5)E在I中燃烧观察到的现象是______________________。
(每空2分、共14分)

(4)2Al+2OH-+2H2O=2AlO2-+3H2↑
AlO2-+CO2+2H2O=HCO3-+Al(OH)3↓
(5)镁条剧烈燃烧,生成白色粉末,反应器内壁附着有黑色的碳
【解析】本题是无机框图题,关键是找准突破点。反应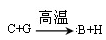 能放出大量的热,该反应曾应用于铁轨的焊接,因此该反应是铝热反应,所以C是铝,B是铁,H是氧化铝,则A就是O,G是氧化铁。I是一种常见的温室气体,所以I是CO2,则D是碳。能在CO2中燃烧且生成碳的单质应该是金属镁,且再氧化镁中镁元素的含量就是60%,所以E是镁,F是氧化镁。
能放出大量的热,该反应曾应用于铁轨的焊接,因此该反应是铝热反应,所以C是铝,B是铁,H是氧化铝,则A就是O,G是氧化铁。I是一种常见的温室气体,所以I是CO2,则D是碳。能在CO2中燃烧且生成碳的单质应该是金属镁,且再氧化镁中镁元素的含量就是60%,所以E是镁,F是氧化镁。
(1)铝热反应的方程式是2Al+Fe2O3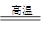 2Fe+Al2O3
2Fe+Al2O3
(2)CO2是直线型结构,电子式是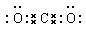 。
。
(3)
(4)金属铝和氢氧化钠溶液反应生成氢气和偏铝酸钠,反应的方程式是2Al+2OH-+2H2O=2AlO2-+3H2↑。向偏铝酸钠溶液中通入过量的CO2,反应的方程式是AlO2-+CO2+2H2O=HCO3-+Al(OH)3↓。
(5)反应时的现象是:镁条剧烈燃烧,生成白色粉末,反应器内壁附着有黑色的碳。

已知下列数据:
下图为实验室制取乙酸乙酯的装置图。
(1)当饱和碳酸钠溶液上方收集到较多液体时,停止加热,取下小试管B,充分振荡,静置。振荡前后的实验现象_________(填选项)。
| A.上层液体变薄 | B.下层液体红色变浅或变为无色 |
| C.有气体产生 | D.有果香味 |
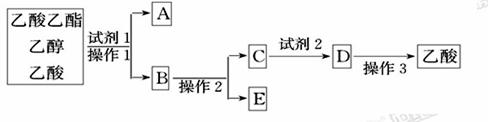
①试剂1最好选用___________;
②操作1是_____,所用的主要仪器名称是________;
③试剂2最好选用___________;
④操作2是___________;
⑤操作3中温度计水银球的位置应为如下图中______(填a、b、c、d)所示,在该操作中,除蒸馏烧瓶、温度计外,还需要的玻璃仪器有_______、_______、_______、______,收集乙酸的适宜温度是___________。