题目内容
17.少量钠应保存在( )| A. | 敞口容器中 | B. | 煤油中 | C. | 水中 | D. | 盐酸中 |
分析 根据金属钠的性质来分析其保存方法:钠性质较活泼,能和空气中的氧气、水等物质反应,所以保存要隔绝空气.
解答 解:A.钠极易和氧气反应生成氧化钠而变质,所以钠不能保存在敞口容器中,故A错误;
B.钠的密度大于煤油的密度,且钠和煤油不反应,所以把钠放置在煤油中而阻止了与氧气和水的反应,故B正确;
C.钠能和水反应生成氢氧化钠和氢气,所以钠不能保存在水中,故C错误;
D.钠能与盐酸反应,生成氯化钠和氢气,故D错误.
故选B.
点评 本题考查金属钠的性质以及保存知识,注意钠性质较活泼,能和空气中的氧气、水等物质反应,所以保存要隔绝空气,难度不大.

练习册系列答案
 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
7.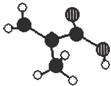 北京东方化工厂生产的某产品只含C、H、O三种元素,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等),下列有关该产品的说法正确的是( )
北京东方化工厂生产的某产品只含C、H、O三种元素,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等),下列有关该产品的说法正确的是( )
 北京东方化工厂生产的某产品只含C、H、O三种元素,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等),下列有关该产品的说法正确的是( )
北京东方化工厂生产的某产品只含C、H、O三种元素,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等),下列有关该产品的说法正确的是( )| A. | 该产品的名称是甲基丙酸 | |
| B. | 该产品与硬脂酸互为同系物 | |
| C. | 四个黑球一定在同一个平面上 | |
| D. | 一定条件下,可以与乙二醇发生酯化反应,也可与氯化氢发生加成反应且产物只有一种 |
8.对于如图所示装置的叙述正确的是( )
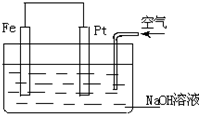

| A. | 这是一个原电池的装置 | |
| B. | 这是电解NaOH溶液的装置 | |
| C. | Pt为正极,其电极反应为:2H++2e-═H2↑ | |
| D. | Fe为负极,其电极反应为:4OH--4e-═2H2O+O2↑ |
12.下列离子的检验不能达到预期目的是( )
| A. | 向待测液里加入NaOH溶液,产生红褐色沉淀,则待测液中肯定含有Fe3+ | |
| B. | 向待测液里加入BaCl2溶液,若产生白色沉淀,再加入过量稀硝酸白色沉淀不溶解,则表明待测液中肯定含有SO42- | |
| C. | 向待测液里加入过量硝酸无现象,再加入硝酸银溶液,若无沉淀生成,则表明待测液中肯定不含Cl- | |
| D. | 向待测液里加入CaCl2溶液,不产生白色沉淀,加入稀盐酸产生无色无味气体,该气体通入澄清石灰水中,溶液变浑浊,则表明待测液中肯定含HCO3- |
9.下列四组溶液混合后,最先出现浑浊的是( )
| 选项 | H2SO4 | Na2S2O3 | H2O |
| A | 5mL0.1mol/L | 5mL0.1mol/L | 0 |
| B | 5mL0.2mol/L | 5mL0.1mol/L | 10 |
| C | 5mL0.3mol/L | 5mL0.1mol/L | 20 |
| D | 5mL0.4mol/L | 5mL0.1mol/L | 30 |
| A. | A | B. | B | C. | C | D. | D |
6.下列关于胶体和溶液的说法中,正确的是( )
| A. | 分散系的分类 | |
| B. | 溶液是电中性的,胶体是带电的 | |
| C. | 光线通过时,溶液产生丁达尔效应,胶体则无丁达尔效应 | |
| D. | 只有胶状物如胶水、果冻类的物质才能称为胶体 |
 (1)NO2-的定性检验:在酸性介质中,NO2-和Fe2+反应产生棕色的[Fe(NO)]2+(N为+2价),反应的离子方程式为2Fe2++NO2-+2H+═Fe3++[Fe(NO)]2++H2O.
(1)NO2-的定性检验:在酸性介质中,NO2-和Fe2+反应产生棕色的[Fe(NO)]2+(N为+2价),反应的离子方程式为2Fe2++NO2-+2H+═Fe3++[Fe(NO)]2++H2O.