题目内容
W、X、Y、Z为短周期内除稀有气体外的4种元素,它们的原子序数依次增大,其中只有Y为金属元素;Z元素的最高正化合价为+6.Y和W的最外层电子数相等.Y、Z两元素原子的质子数之和为W、X两元素质子数之和的3倍.由此可知:
(1)写出元素符号:W为
(2)Y2Z是由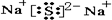
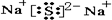 ;
;
(3)由Y、X、W组成的物质中有
(4)用电子式表示Z与钙形成化合物的过程
 .
.
(1)写出元素符号:W为
H
H
,X为O
O
,Y为Na
Na
,Z为S
S
;(2)Y2Z是由
离子键
离子键
键组成的物质,其电子式为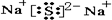
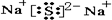
(3)由Y、X、W组成的物质中有
离子
离子
键和共价
共价
键,形成的是离子
离子
化合物;(4)用电子式表示Z与钙形成化合物的过程


分析:短周期的金属只有Li、Be、Na、Mg、Al,Y和W的最外层电子数相等即W和Y同族,所以W只能是H(氢),因不存在稀有气体,所以如果Y是Li,X就成了稀有气体,不成立,所以Y是Na,Y的质子数是11,W的质子数是1,X的质子数有可能是5,6,7,8,9,那么Y+Z就应该有18,21,24、27,30等可能,但Z一定大于Y,也就是12以上,算到最大的短周期元素Cl也只有17,加起来是28,那么Y+Z就一定小于等于28,28不是3的倍数,有24,27两解:1,7,11,13(铝)不成立,1,8,11,16 成立,所以W、X、Y、Z分别为:H,O,Na,S.然后根据问题回答.
解答:解:短周期的金属只有Li、Be、Na、Mg、Al,Y和W的最外层电子数相等即W和Y同族,所以W只能是H(氢),因不存在稀有气体,所以如果Y是Li,X就成了稀有气体,不成立,所以Y是Na,Y的质子数是11,W的质子数是1,X的质子数有可能是5,6,7,8,9,那么Y+Z就应该有18,21,24、27,30等可能,但Z一定大于Y,也就是12以上,算到最大的短周期元素Cl也只有17,加起来是28,那么Y+Z就一定小于等于28,28不是3的倍数,有24,27两解:1,7,11,13(铝)不成立,1,8,11,16 成立,所以W、X、Y、Z分别为:H,O,Na,S.
(1)W、X、Y、Z分别为:H,O,Na,S,故答案为:H;O;Na;S;
(2)Na2S是由钠离子和硫离子通过离子键组成的物质,其电子式为: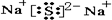 ,故答案为:离子键;
,故答案为:离子键;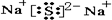 ;
;
(3)NaOH中钠离子和氢氧根离子之间存在离子键,氢氧根离子中氧原子和氢原子之间存在共价键,NaOH为离子化合物,故答案为:离子;共价;离子.
(4)用电子式表示CaS的形成过程为: ,故答案为:
,故答案为: .
.
(1)W、X、Y、Z分别为:H,O,Na,S,故答案为:H;O;Na;S;
(2)Na2S是由钠离子和硫离子通过离子键组成的物质,其电子式为:
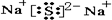 ,故答案为:离子键;
,故答案为:离子键;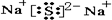 ;
;(3)NaOH中钠离子和氢氧根离子之间存在离子键,氢氧根离子中氧原子和氢原子之间存在共价键,NaOH为离子化合物,故答案为:离子;共价;离子.
(4)用电子式表示CaS的形成过程为:
 ,故答案为:
,故答案为: .
.点评:本题考查原子结构与元素周期律的关系,题目难度中等,正确推断元素的种类为解答该题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
X、Y、Z、W为短周期主族元素,原子序数依次增大,X的族序数是周期数的2倍,Y的气态氢化物与最高价氧化物水化物可形成盐,Z的最外层电子数与其电子总数比为3:8,下列说法正确的是( )
| A、X、Y、W的最高价含氧酸酸性顺序:Y>W>X | B、气态氢化物的稳定性:Z>W | C、X、W形成的化合物XW4属于离子化合物 | D、原子半径:Z>W>X>Y |

