题目内容
【题目】把足量熟石灰放入蒸馏水中,一段时间后达到平衡:Ca(OH)2(s)![]() Ca2+(aq)+2OH-(aq),下列叙述不正确的是( )
Ca2+(aq)+2OH-(aq),下列叙述不正确的是( )
A.给溶液加热,Ca(OH)2的溶解度减小
B.向溶液中加入少量CaO充分反应后,恢复到原温度,溶液的pH升高
C.温度不变,向溶液中加入少量Na2CO3固体,充分反应后,Ksp[Ca(OH)2]不变
D.向溶液中加入少量的NaOH固体,Ca(OH)2固体增多
【答案】B
【解析】
A. Ca(OH)2的溶解度随温度的升高而降低,给溶液加热,Ca(OH)2的溶解度减小,A正确;
B. 恒温下向溶液中加入CaO,发生反应:CaO+H2O=Ca(OH)2,消耗溶液中的水,析出Ca(OH)2固体,但溶液仍为该温度下的饱和溶液,溶液的pH不变,B错误;
C. 温度不变,向溶液中加入少量Na2CO3固体,该平衡向左移动,但物质的溶度积只与温度有关,与物质的浓度无关,因此充分反应后,Ksp[Ca(OH)2]不变,C正确;
D. 加入少量的NaOH固体,NaOH电离产生OH-,使溶液中OH-浓度增大,溶解平衡逆向移动,最终达到平衡时溶液中Ca(OH)2固体增多,D正确;
故合理选项是B。

【题目】砂质土壤分析中常用 Karl Fischer法是测定其中微量水含量,该方法是利用I2和SO2反应定量消耗水作为原理(假设土壤中其他成分不参加反应),据此回答下列问题:
(1)写出该反应的化学反应方程式:_______________________。
步骤I:反应样品中的水
下图是某同学在实验室模拟Karl Fischer法的实验装置图:
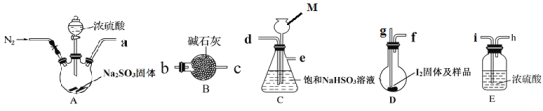
(2)装置连接的顺序为a→____________(填接口字母顺序);M仪器的名称为________________,其在实验过程中的作用是:____________;
(3)操作步骤为:①连接装置并检查装置气密性,②装入药品,____________________;③关闭弹簧夹,打开分液漏斗活塞;④反应结束后,关闭分液漏斗活塞,继续通入N2,⑤取下D装置,···
步骤④中继续通入N2的目的是________________________________
步骤 II:测定剩余的碘
向反应后的D装置加入蒸馏水,过滤,充分洗涤,并合并洗涤液和滤液,将其配成250.00mL溶液,取25.00mL用0.20mol·L-1 Na2S2O3标准液滴定剩余的I2单质,已知反应如下:2S2O32-+I2=S4O62-+2I-。
(4)Na2S2O3标准液应装在_____________(填“酸式”、“碱式”)滴定管中;上述操作中,合并洗涤液和滤液的目的是__________________________;
(5)滴定实验重复四次得到数据如下:
实验 | ① | ② | ③ | ④ |
消耗的标准液的体积/mL | 18.37 | 20.05 | 19.95 | 20.00 |
①若实验开始时,向D装置中加入10.00 g土壤样品和10.16克I2(已知I2过量),则样品土壤中水的含量为_________%。
②若Na2S2O3标准液已部分氧化变质,则水含量测定结果将____________(填“偏高”、“ 偏低”或“不变”)。