题目内容
|
在标准状况下,将2.24 L NH3与4.48 L HCl气体充入密闭容器内混合,下列说法正确的是 | |
A. |
反应中有0.5NA个极性共价键断裂 |
B. |
反应中有0.4NA个极性共价键形成,有0.1NA个离子键形成 |
C. |
混合后,容器内物质含有0.5NA个化学键 |
D. |
混合前气体中含有0.4NA个极性共价键 |
答案:B
解析:
解析:
|
据反应NH3+HCl |

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
在标准状况下,将2.8 g铁和2.3 g钠分别与100 m L 1 mol·L-1的盐酸反应 ,则放出H2的体积( )
| A.铁和钠放出一样多 | B.铁的多 | C.钠的多 | D.无法比较 |
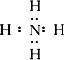 ]+[
]+[