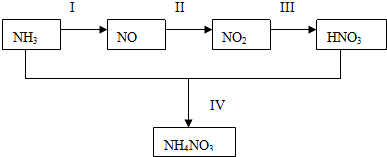
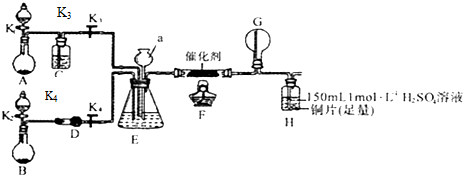
题目内容
1.下列事实一定能证明HNO2是弱电解质的是( )①常温下NaNO2溶液的pH大于7
②用HNO2溶液做导电实验,灯泡很暗
③HNO2和NaCl不能发生反应
④0.1mol•L-1 HNO2溶液的pH=2.1
⑤NaNO2和H3PO4反应,生成HNO2
⑥0.1mol•L-1 HNO2溶液稀释至100倍,pH变化值小于2.
| A. | ①④⑥ | B. | ①②③④ | C. | ①④⑤⑥ | D. | 全部 |
分析 强弱电解质的根本区别是电解质的电离程度,完全电离的电解质是强电解质、部分电离的电解质是弱电解质,要证明亚硝酸是弱电解质,只要能说明亚硝酸部分电离即可,据此分析解答.
解答 解:①常温下NaNO2溶液的pH大于7,说明亚硝酸钠是强碱弱酸盐,则亚硝酸是弱酸,故正确;
②用HNO2溶液做导电实验,灯泡很暗,说明溶液中离子浓度很小,但不能说明亚硝酸部分电离,所以不能证明亚硝酸是弱电解质,故错误;
③HNO2和NaCl不能发生反应,说明不符合复分解反应条件,但不能说明亚硝酸部分电离,所以不能证明亚硝酸是弱电解质,故错误;
④0.1mol•L-1 HNO2溶液的pH=2.1,说明亚硝酸部分电离,则亚硝酸是弱电解质,故正确;
⑤NaNO2和H3PO4反应,生成HNO2,根据强酸制取弱酸知,磷酸酸性大于亚硝酸,磷酸是中强酸,则亚硝酸是弱酸,故正确;
⑥0.1mol•L-1 HNO2溶液稀释至100倍,pH变化值小于2,说明亚硝酸中存在电离平衡,则亚硝酸是弱酸,为电解质,故正确;
故选C.
点评 本题考查强弱电解质判断,为高频考点,明确强弱电解质本质区别是解本题关键,根据电解质电离程度判断电解质强弱,不能根据其水溶液导电性强弱判断,题目难度不大.

练习册系列答案
相关题目
11.下列仪器中,没有零刻度的是( )
| A. | 托盘天平 | B. | 滴定管 | C. | 温度计 | D. | 容量瓶 |
12.将4mol 甲烷与氯气发生取代反应,待反应完全后测知四种取代物物质的量相同,测消耗的氯气有( )
| A. | 2mol | B. | 10mol | C. | 7.5mol | D. | 6mol |
16.下列描述中不符合生产实际的是( )
| A. | 电解熔融Al2O3制金属铝,用铁作阳极 | |
| B. | 电解法精炼粗铜,用纯铜作阴极 | |
| C. | 电解饱和食盐水制烧碱,用涂镍碳钢网作阴极 | |
| D. | 在镀件上镀锌,用锌用阳极,硫酸锌作电解质溶液 |
10.下列有关化学反应速率的说法不正确的是( )
| A. | 升高温度,可以加快反应速率,缩短可逆反应达到平衡的时间 | |
| B. | 化学反应达到最大限度时,正逆反应速率也达到最大且相等 | |
| C. | 用锌和稀硫酸反应制取H2时,滴加几滴硫酸铜溶液能加快反应速率 | |
| D. | 用铁片和稀硫酸反应制H2比用98%的浓硫酸产生H2的速率快 |
11.为探究铁钉和钢钉在碱性溶液中遇到高锰酸钾时是否存在电化学腐蚀,进行下图所示实验.下列推断正确的是( )

| A. | 钢钉表面有白色沉淀 | B. | 实验2中的高锰酸钾溶液先变色 | ||
| C. | 负极的电极反应为:Fe-3e-→Fe3+ | D. | 铁钉表面有红褐色物质生成 |