题目内容
7.下列物质中所含原子数最多的是( )| A. | 0.3 molSO3 | B. | 44gCO2 | ||
| C. | 6.02×1023个NH3分子 | D. | 4℃时18mL的水 |
分析 A、0.3 molSO3原子的物质的量为:4×0.3mol=1.2mol;
B、44gCO2原子的物质的量为:$\frac{44g}{44g/mol}×3$=3mol;
C、6.02×1023个NH3中原子物质的量是:$\frac{6.02×1{0}^{23}}{6.02×1{0}^{23}}$×4=4mol;
D、根据m=ρV计算水的质量,根据n=$\frac{N}{{N}_{A}}$计算H2O的物质的量,每个H2O分子含有3个原子,原子的物质的量为H2O的3倍.
解答 解:A、0.3 molSO3原子的物质的量为:4×0.3mol=1.2mol;
B、44gCO2原子的物质的量为:$\frac{44g}{44g/mol}×3$=3mol;
C、6.02×1023个NH3中原子物质的量是:$\frac{6.02×1{0}^{23}}{6.02×1{0}^{23}}$×4=4mol;
D、4℃时18ml的水的质量为18ml×1g/ml=18g,物质的量为$\frac{18g}{18g/mol}$=1mol,每个H2O分子含有3个原子,含有原子的物质的量为3mol;原子的物质的量最大的是4mol,
故选:C.
点评 本题考查物质的量的有关计算,把握质量、物质的量、体积、微粒数的关系及分子构成为解答的关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.将某些化学知识用图象表示,可以收到直观、简明的效果.下列图象所表示的化学知识中,
明显不正确的是( )
明显不正确的是( )
| A. | 分散系的分类 | B. | 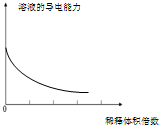 稀释浓氢氧化钠溶液的过程 | ||
| C. | 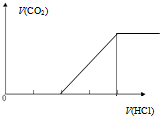 向碳酸钠溶液中逐滴滴加盐酸 | D. | 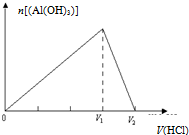 向偏铝酸钠溶液中逐滴滴加盐酸 |
15.已知在101kPa时:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-820kJ•mol-1,则下列说法正确的是( )
| A. |  反应过程中的能量变化关系可用如图表示 | |
| B. | CH4的燃烧热是820kJ | |
| C. | 11.2L(标准状况)CH4完全燃烧生成气态水时放出410kJ热量 | |
| D. | 该反应发生断裂的化学键只有极性键 |
2.在实验室里可按如图所示装置干燥并收集气体R,且吸收多余的R,则R是( )


| A. | CH4 | B. | HCl | C. | NO | D. | NH3 |
12.下列污染现象主要与SO2有关的是( )
| A. | 臭氧空洞 | B. | 雾霾 | C. | 温室效应 | D. | 酸雨 |
19.表示正反应是吸热反应的图象是( )
| A. |  | B. |  | C. |  | D. |  |
16.下列情境中溶液的导电能力没有经过“先减弱后增强”变化的是(忽略溶液体积的变化)( )
| A. | 向饱和硫化氢溶液中持续通入SO2 | |
| B. | 向硫酸铝溶液中持续加入氢氧化钡固体 | |
| C. | 向Ca(HCO3)2溶液中滴加澄清石灰水至过量 | |
| D. | 向氯化铁溶液中持续通入SO2 |
7.下列物质中,不属于合金的是( )
| A. | 硬铝 | B. | 黄铜 | C. | 纯铁 | D. | 生铁 |
 常温下,A是双原子分子气态单质,其密度为3.17g/L(标准标况下),B、C、D都是含A元素的化合物,转化关系如图所示:
常温下,A是双原子分子气态单质,其密度为3.17g/L(标准标况下),B、C、D都是含A元素的化合物,转化关系如图所示: