题目内容
化学在能源开发与利用中起着十分重要的作用.(1)蕴藏在海底的“可燃冰”是高压下形成的外观酷似冰的甲烷水合物.我国南海海底有丰富的“可燃冰”资源.取365g分子式为CH4?9H2O的“可燃冰”,将其释放的甲烷完全燃烧生成CO2和H2O(l),可放出1780.6kJ的热量,则甲烷燃烧的热化学方程式为 .
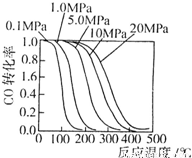
(2)甲醇是重要的基础化工原料,又是一种新型的燃料,制取甲醇的传统方法是采用CuO-ZnO/γ-Al2O3为催化剂,合成反应为:CO+2H2
 CH3OH.生产中一些工艺参数如图所示.该反应为 (填“吸热”或“放热”)反应.说明你作出判断的依据 .
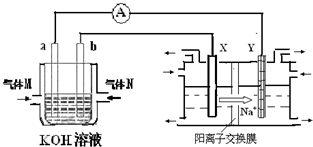
CH3OH.生产中一些工艺参数如图所示.该反应为 (填“吸热”或“放热”)反应.说明你作出判断的依据 .最近有人制造了一种燃料电池,一个电极通入空气,另一个电极加入甲醇,电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-离子.该电池的正极反应式为 .电池工作时,固体电解质里的O2-向 极推动.
【答案】分析:(1)根据热化学方程式的书写方法;
(2)根据温度对化学平衡的影响;
(3)根据原电池原理,正极O2得到电子生成负极O2-;电池中阴离子向负极移动.
解答:解:(1)365g中甲烷的物质的量为 =2mol,其完全燃烧生成CO2和H2O(l),可放出1780.6kJ的热量,则1mol甲烷其完全燃烧放出热量890.3 kJ,则甲烷燃烧的热化学方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3 kJ?mol-1,故答案为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3 kJ?mol-1;
=2mol,其完全燃烧生成CO2和H2O(l),可放出1780.6kJ的热量,则1mol甲烷其完全燃烧放出热量890.3 kJ,则甲烷燃烧的热化学方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3 kJ?mol-1,故答案为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3 kJ?mol-1;
(2)由图可知:论在何种压强下,都是温度越高,CO的转化率越小,说明正反应放热,
故答案为:放热;由图知,不论在何种压强下,都是温度越高,CO的转化率越小;
(3)根据原电池原理,正极O2得到电子生成负极O2-:O2+4e-=2O2-,电池中阴离子向负极移动,故答案为:O2+4e-=2O2-;负.
点评:本题考查热化学方程式的书写,电极方程式的书写等,要能根据题目所给信息解题,善于发掘题目信息.
(2)根据温度对化学平衡的影响;
(3)根据原电池原理,正极O2得到电子生成负极O2-;电池中阴离子向负极移动.
解答:解:(1)365g中甲烷的物质的量为
 =2mol,其完全燃烧生成CO2和H2O(l),可放出1780.6kJ的热量,则1mol甲烷其完全燃烧放出热量890.3 kJ,则甲烷燃烧的热化学方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3 kJ?mol-1,故答案为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3 kJ?mol-1;
=2mol,其完全燃烧生成CO2和H2O(l),可放出1780.6kJ的热量,则1mol甲烷其完全燃烧放出热量890.3 kJ,则甲烷燃烧的热化学方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3 kJ?mol-1,故答案为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3 kJ?mol-1;(2)由图可知:论在何种压强下,都是温度越高,CO的转化率越小,说明正反应放热,
故答案为:放热;由图知,不论在何种压强下,都是温度越高,CO的转化率越小;
(3)根据原电池原理,正极O2得到电子生成负极O2-:O2+4e-=2O2-,电池中阴离子向负极移动,故答案为:O2+4e-=2O2-;负.
点评:本题考查热化学方程式的书写,电极方程式的书写等,要能根据题目所给信息解题,善于发掘题目信息.

练习册系列答案
相关题目
 化学在能源开发与利用中起到十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.
化学在能源开发与利用中起到十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料. 化学在能源开发与利用中起着十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.
化学在能源开发与利用中起着十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.

 2NH3 (g) ΔH=-92.2kJ·mol-1
2NH3 (g) ΔH=-92.2kJ·mol-1