题目内容
11.设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )| A. | 标准状况下,1L乙烷所含有的分子数为NA/22.4 | |
| B. | 1mol甲基(-CH3)所含电子数为9NA | |
| C. | 常温下,28g C2H4含NA个碳碳双键 | |
| D. | 1L0.1mol•L-1乙酸溶液中H+数为0.1NA |
分析 A、根据分子数N=$\frac{V}{{V}_{m}}{N}_{A}$来计算;
B、甲基不带电荷;
C、求出乙烯的物质的量,然后根据1mol乙烯中含1mol碳碳双键来分析;
D、乙酸是弱电解质.
解答 解:A、标况下,1L乙烷分子数N=$\frac{V}{{V}_{m}}{N}_{A}$=$\frac{1L}{22.4L/mol}{N}_{A}/mol$=$\frac{{N}_{A}}{22.4}$,故A正确;
B、甲基不带电荷,故1mol甲基含9mol电子即9NA个,故B正确;
C、28g乙烯的物质的量为1mol,而1mol乙烯中含1mol碳碳双键即NA个碳碳双键,故C正确;
D、乙酸是弱电解质,在溶液中不能完全电离,故溶液中的氢离子的个数小于0.1NA个,故D错误.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,掌握物质的性质和结构是解题关键.

练习册系列答案
相关题目
1.下列说法正确的是( )
| A. | 氯化铁溶液有较强氧化性,故可用作净水剂 | |
| B. | 煤中含有大量的有机物,用干馏的方法通过发生物理变化得到产物 | |
| C. | 除去CH4中的少量C2H4:通过盛有酸性高锰酸钾溶液的洗气瓶 | |
| D. | 将ag铜丝灼烧成黑色后趁热插入乙醇中,铜丝变红,再次称量质量等于a g |
2.下列化合物中为离子化合物的是( )
| A. | CH4 | B. | O3 | C. | 盐酸 | D. | 氯化钾 |
6.化合物M结构如图所示.对化合物M的叙述正确的是( )


| A. | M的分子式为C12H12O5 | |
| B. | M只能与溴水发生加成反应 | |
| C. | 1mol M最多可和5mol H2发生加成反应 | |
| D. | 1molM最多可消耗3molNaOH |
3.下列液体中,易溶于水的是( )
| A. | 汽油 | B. | 乙醇 | C. | 乙酸乙酯 | D. | 苯 |
20.下列关于燃料的说法错误的是( )
| A. | 煤可以气化得到发生炉煤气、水煤气、焦炉气,这些气体都含有CO | |
| B. | 液化石油气的成分不同于天然气,容易冒黑烟 | |
| C. | 沼气因使用具有危险性,不能推广使用 | |
| D. | 燃料电池能源的利用率高、污染少,具有很好的应用前景 |
1. 科学家根据自然界存在的N2制取出N3,又陆续制取出N5+、N4H44+等离子.已知N4H44+的空间构型如图,下列说法正确的是( )
科学家根据自然界存在的N2制取出N3,又陆续制取出N5+、N4H44+等离子.已知N4H44+的空间构型如图,下列说法正确的是( )
 科学家根据自然界存在的N2制取出N3,又陆续制取出N5+、N4H44+等离子.已知N4H44+的空间构型如图,下列说法正确的是( )
科学家根据自然界存在的N2制取出N3,又陆续制取出N5+、N4H44+等离子.已知N4H44+的空间构型如图,下列说法正确的是( )| A. | N3和N2互为同位素 | |
| B. | 7.0gN5+离子含有34×6.02×1022个电子 | |
| C. | N5+中氮、氮原子间形成离子键 | |
| D. | N4H44+的4个H共平面 |

 ;名称是环己烷.
;名称是环己烷.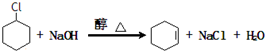 .
. +Br2→
+Br2→ .
. +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ +2NaBr+2H2O.
+2NaBr+2H2O.