题目内容
18.下列各组元素性质的递变情况错误的是( )| A. | Na、Mg、Al原子最外层电子数依次增多 | |
| B. | N、O、F元素最高正价依次增大 | |
| C. | Na、K、Rb电负性逐渐减小 | |
| D. | P、S、Cl元素最高价含氧酸酸性依次增强 |
分析 A、根据Na、Mg、Al原子的核外电子排布分析;
B、最外层电子数目=元素的最高正价(氧、氟除外);
C、同主族元素从上到下元素的电负性逐渐减弱;
D、非金属性越强最高价氧化物对应水化物的酸性越强.
解答 解:A、Na、Mg、Al原子的核外电子分别为11、12、13,原子最外层电子数分别为1、2、3,逐渐增多,故A正确;
B、氧、氟无正价,只有零价和负价,故B错误;
C、同主族元素从上到下元素的电负性依次减弱,则Na、K、Rb元素的电负性逐渐减小,故C正确;
D、非金属性:P<S<Cl,所以酸性:P、S、Cl元素最高价含氧酸酸性依次增强,故D正确;
故选B.
点评 本题考查元素周期律的递变规律,题目难度不大,注意把握元素周期律的递变规律与元素在周期表中的位置关系.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
9.下列说法正确的是( )
| A. | 根据分散系的稳定性,将分散系分为溶液、胶体和浊液 | |
| B. | 根据是否具有丁达尔效应鉴别蛋白质溶液和氯化钠溶液 | |
| C. | 在饱和氯化铁溶液中逐滴加入NaOH溶液,生成Fe(OH)3胶体 | |
| D. | “纳米材料”是粒子直径为1 nm~100 nm的材料,纳米铜是其中的一种,它是胶体 |
6.正确掌握化学用语是学好化学的基础,下列有关表述正确的是( )
| A. | F-的结构示意图: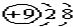 | |
| B. | 乙烷和丙烯互为同系物 | |
| C. | NaCl的电子式:Na${\;}_{×}^{•}$$\underset{\stackrel{••}{Cl}}{••}$${\;}_{•}^{•}$ | |
| D. | H2、D2、T2属于同位素,化学性质几乎完全相同 |
13.有一种纽扣微型电池,其电极分别是Ag2O和Zn.电解池是KOH溶液,所以俗称银锌电池,该电池的电极反应式为:Zn+2OH--2e-═Zn(OH)2,Ag2O+H2O+2e-═2Ag+2OH-下列说法,正确的是( )
| A. | 锌为负极,Ag2O为正极? | B. | 放电时,正极附近pH值上升? | ||
| C. | 放电时,电子由Ag2O流向Zn | D. | 放电时,负极附近溶液pH值升高 |
3.下列各组物质中,将前者加入后者时,无论前者是否过量,都能用同一个化学方程式表示的是( )
| A. | 稀盐酸,Na2CO3溶液 | B. | 稀H2SO4溶液,NaAlO2溶液 | ||
| C. | Cl2,NaBr溶液 | D. | CO2,澄清石灰水 |
10.下列实验用来证明SO2的存在,其中正确的是( )
| A. | 能使品红褪色 | |
| B. | 能使湿润的蓝色石蕊试纸变红 | |
| C. | 通入足量的NaOH溶液中,再滴入BaCl2溶液有白色沉淀生成,该沉淀溶于稀盐酸 | |
| D. | 通入稀溴水中能使溴水褪色,得澄清溶液,再滴加Ba(NO3)2溶液有白色沉淀,该沉淀不溶于硝酸 |
7.有机物的结构简式如图所示 ,该有机物的分子式为( )
,该有机物的分子式为( )
 ,该有机物的分子式为( )
,该有机物的分子式为( )| A. | C14H24O2 | B. | C15H23O2 | C. | C16H24O2 | D. | C15H24O2 |

 $\stackrel{△}{→}$
$\stackrel{△}{→}$
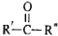 →
→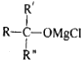 $\stackrel{H_{2}O}{→}$
$\stackrel{H_{2}O}{→}$


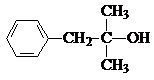


 实验室需要0.1mol•L-1 NaOH溶液450mL和0.5mol•L-1硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题:
实验室需要0.1mol•L-1 NaOH溶液450mL和0.5mol•L-1硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题: