题目内容
14.下列说法错误的是( )| A. | 从1L 1 mol•L-1 的氯化钠溶液中取出10ml后,其浓度仍是1 mol•L-1 | |
| B. | NaHSO4溶液与NaOH溶液反应的离子方程式:H++OH-═H2O | |
| C. | 黄河入海口处三角洲的形成与胶体性质无关 | |
| D. | 氧化剂具有氧化性,在化学反应中化合价降低,发生还原反应 |
分析 A.溶液是均一的,取出溶液、剩余溶液浓度均与原溶液浓度相等;
B.NaHSO4溶液与NaOH溶液反应生成硫酸钠与水,溶液中NaHSO4完全电离为钠离子、氢离子与硫酸根,NaOH电离为离子与氢氧根离子,本质是氢离子与氢氧根离子结合生成水;
C.黄河入海口处三角洲的形成是胶体聚沉结果;
D.氧化剂具有氧化性,在化学反应中所含元素化合价降低,发生还原反应.
解答 解:A.溶液是均一的,取出10mL溶液与原溶液浓度相等,其浓度仍是1 mol•L-1,故A正确;
B.NaHSO4溶液与NaOH溶液反应生成硫酸钠与水,溶液中NaHSO4完全电离为钠离子、氢离子与硫酸根,NaOH电离为离子与氢氧根离子,本质是氢离子与氢氧根离子结合生成水,反应的离子方程式:H++OH-═H2O,故B正确;
C.黄河入海口处三角洲的形成是胶体聚沉结果,与与胶体性质无关,故C错误;
D.氧化剂具有氧化性,在化学反应中所含元素化合价降低,发生还原反应,故D正确,
故选:C.
点评 本题考查溶液性质、离子方程式、胶体性质、氧化还原反应,比较基础,注意对基础知识的理解掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.正确的实验操作是实验成功的重要因素,下列实验操作正确的是( )
| A. | 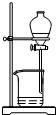 放出碘的苯溶液 放出碘的苯溶液 | B. | 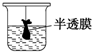 分离或提纯胶体 分离或提纯胶体 | ||
| C. | 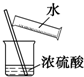 实验室稀释浓硫酸 实验室稀释浓硫酸 | D. | 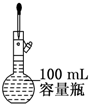 定容 定容 |
19.下列说法正确的是( )
| A. | 摩尔是国际单位制中的7 个基本物理量之一 | |
| B. | 硫酸的摩尔质量是98 g | |
| C. | 0.5molH2 约含有3.01×1023个氢原子 | |
| D. | NA个氧气分子与NA 个氢气分子的质量比为16:1 |
6.某溶液经分析,其中只含Na+、K+、Mg2+、Cl-、SO42-,已知其中Na+、K+、Mg2+、Cl-的浓度均为0.1mol•L-1,则SO42- 的物质的量浓度为( )
| A. | 0.1 mol•L-1 | B. | 0.15 mol•L-1 | C. | 0.2 mol•L-1 | D. | 0.3 mol•L-1 |
3.下列各组性质的比较中,不正确的是( )
| A. | 碱性:NaOH>Mg(OH)2 | B. | 热稳定性:HCl>HBr | ||
| C. | 失电子能力:K>Na | D. | 原子半径:CI>S |
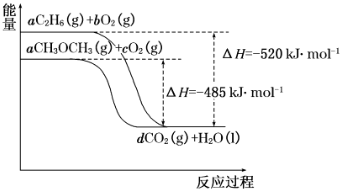
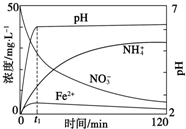 工、农业废水及生活污水中浓度较高的NO${\;}_{3}^{-}$会造成氮污染,工业上处理水体中NO${\;}_{3}^{-}$的一种方法是单质铁化学还原法.某化学小组用废铁屑和硝酸盐溶液模拟此过程,实验如下.
工、农业废水及生活污水中浓度较高的NO${\;}_{3}^{-}$会造成氮污染,工业上处理水体中NO${\;}_{3}^{-}$的一种方法是单质铁化学还原法.某化学小组用废铁屑和硝酸盐溶液模拟此过程,实验如下.