题目内容
【题目】阿斯巴甜作为强烈甜味剂被广泛应用于食品、饮料、糖果等,工业上可以用苯丙氨酸甲酯和α﹣氨基丁二酸为原料合成: 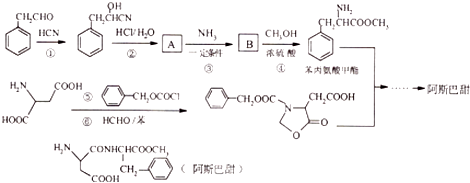
已知:RCN ![]() RCOOH;
RCOOH; ![]()
![]()
![]()
(1)A中含氧官能团的名称为;
(2)①、⑤的反应类型依次为、;
(3)B的同分异构体中同时符合下列条件的有2种,写出其结构简式;
①有三种化学环境不同的氢原子;②含苯环的中性物质
(4)写出阿斯巴甜与足量NaOH水溶液充分反应的化学方程式;
(5)写出以1,3﹣丙二醇(HOCH2﹣CH2﹣CH2OH)为原料制备 ![]() 的合成路线流程(无机试剂任选).合成路线流程示例如下 CH2═CH3
的合成路线流程(无机试剂任选).合成路线流程示例如下 CH2═CH3 ![]() CH3CH2Br
CH3CH2Br ![]() CH3CH2OH: .
CH3CH2OH: .
【答案】
(1)羟基、羧基
(2)加成;取代
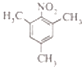
(3)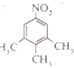 、
、 
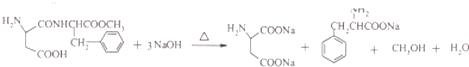
(4)
(5)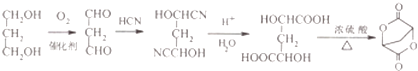
【解析】解:(1.)根据题中已知的条件,可知反应②是将反应物中的﹣CN变成﹣COOH,所以A的结构简式为 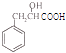 ,所以答案是:羟基、羧基;
,所以答案是:羟基、羧基;
(2.)反应①是醛基与HCN加成,生成羟基腈,反应⑤氨基中的一个H被 ![]() 取代所以答案是:加成;取代;
取代所以答案是:加成;取代;
(3.)  与氨气反应生成的B为
与氨气反应生成的B为 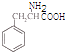 ,有三种化学环境不同的氢原子说明分子很对称三个碳分布在苯环的间位,中性物质说明氮原子形成了硝基,据此可以写出结构简式为:
,有三种化学环境不同的氢原子说明分子很对称三个碳分布在苯环的间位,中性物质说明氮原子形成了硝基,据此可以写出结构简式为: 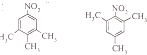 ,所以答案是:
,所以答案是: 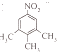 、
、 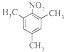 ;
;
(4.)阿斯巴甜与足量NaOH水溶液充分反应,其中酯基和肽键能水解,羧基被中和,所有方程式: 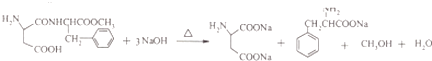 ,
,
所以答案是: 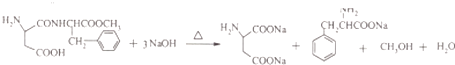 ;
;
(5.)根据产物 ![]() 和原料(HOCH2﹣CH2﹣CH2OH)比较要知,碳原子数增加了两个,且产物是一个很对称的结构,将产物水解后得到
和原料(HOCH2﹣CH2﹣CH2OH)比较要知,碳原子数增加了两个,且产物是一个很对称的结构,将产物水解后得到 ![]() ,再对比原料可知,在原料上再引入两个碳原子,可以参照题目流程中的第①②步骤,可以达到目的,写出的流程为:
,再对比原料可知,在原料上再引入两个碳原子,可以参照题目流程中的第①②步骤,可以达到目的,写出的流程为: 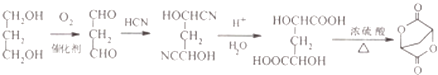 ,
,
所以答案是: 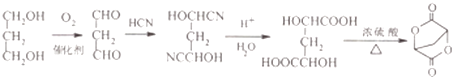 .
.
【考点精析】根据题目的已知条件,利用有机物的结构和性质的相关知识可以得到问题的答案,需要掌握有机物的性质特点:难溶于水,易溶于汽油、酒精、苯等有机溶剂;多为非电解质,不易导电;多数熔沸点较低;多数易燃烧,易分解.

 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案【题目】为提纯下列物质(括号内物质为杂质),所选用的试剂和分离方法正确的是
物质 | 除杂试剂 | 分离方法 | |
A | 硝酸铜溶液(硝酸银) | 铜粉 | 结晶 |
B | Cl2(HCl) | NaOH溶液 | 洗气 |
C | Br2(H2O) | 酒精 | 萃取 |
D | 铜粉(铁粉) | 稀盐酸 | 过滤 |
A. A B. B C. C D. D
【题目】高炉炼铁是冶炼铁的主要方法,发生的主要反应为:
Fe2O3(s)+3CO(g)2Fe(s)+3CO2(g)△H=a kJ mol﹣1
(1)已知:①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H1=+489.0kJ mol﹣1
②C(石墨)+CO2(g)=2CO(g)△H2=+172.5kJ mol﹣1
则a=kJ mol﹣1 .
(2)冶炼铁反应的平衡常数表达式K= , 温度升高后,K值(填“增大”、“不变”或“减小”).
(3)在T℃时,该反应的平衡常数K=64,在2L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡.
Fe2O3 | CO | Fe | CO21 | |
甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
乙/mol | 1.0 | 2.0 | 1.0 | 1.0 |
①甲容器中CO的平衡转化率为 .
②下列说法正确的是(填字母).
a.若容器内气体密度恒定时,标志反应达到平衡状态 b.甲容器中CO的平衡转化率大于乙的
c.甲、乙容器中,CO的平衡浓度之比为2:3 d.增加Fe2O3可以提高CO的转化率
(4)采取一定措施可防止钢铁腐蚀.下列装置中的烧杯里均盛有等浓度、等体积的NaCl溶液.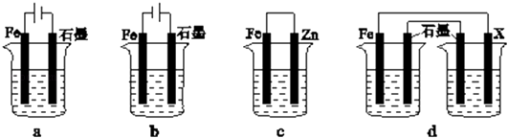
①在a~c装置中,能保护铁的是(填字母).
②若用d装置保护铁,X极的电极材料应是(填名称).