题目内容
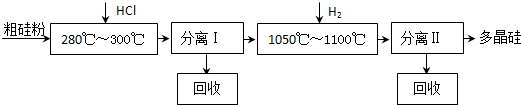
我国目前广泛应用三氯氢硅氢还原法制备多晶硅。制备三氯氢硅的反应为:
Si(s)+3HCl(g) == SiHCl3(g)+H2(g) ΔH=-210 kJ/mol。
伴随的副反应有:Si(s)+4HCl(g) == SiCl4(g)+2H2(g) ΔH=-241 kJ/mol。
SiCl4在一定条件下与H2反应可转化为SiHCl3,反应的热化学方程式为:
A.SiCl4+H2 == SiHCl3+HCl ΔH= +31 kJ/mol
B.SiCl4+H2 == SiHCl3+2HCl ΔH= -31 kJ/mol
C.SiCl4(g)+H2(g) == SiHCl3(g)+HCl(g) ΔH=+31 kJ/mol
D.SiCl4(g)+H2(g) == SiHCl3(g)+2HCl(g) ΔH= -31 kJ/mol
【答案】
C
【解析】略

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
我国目前广泛应用三氯氢硅氢还原法制备多晶硅。制备三氯氢硅的反应为:
Si(s)+3HCl(g) ="=" SiHCl3(g)+H2(g) ΔH="-210" kJ/mol。
伴随的副反应有:Si(s)+4HCl(g) ="=" SiCl4(g)+2H2(g) ΔH="-241" kJ/mol。
SiCl4在一定条件下与H2反应可转化为SiHCl3,反应的热化学方程式为:
| A.SiCl4+H2 ="=" SiHCl3+HClΔH=" +31" kJ/mol |
| B.SiCl4+H2 ="=" SiHCl3+2HCl ΔH=" -31" kJ/mol |
| C.SiCl4(g)+H2(g) ="=" SiHCl3(g)+HCl(g) ΔH="+31" kJ/mol |
| D.SiCl4(g)+H2(g) ="=" SiHCl3(g)+2HCl(g) ΔH=" -31" kJ/mol |