题目内容
往含0.2 mol NaOH和0.1 mol Ba(OH)2的溶液中持续稳定地通入CO2气体,当通入气体的体积为6.72 L(标准状况下)时立即停止,则在这一过程中,溶液中离子数目和通入CO2气体的体积关系正确的图像是(气体的溶解忽略不计)
C
解析

练习册系列答案
相关题目
有关化学用语正确的是 ( )
| A.溴乙烷的分子式C2H5Br |
| B.乙醇的结构简式C2H6O |
C.四氯化碳的电子式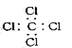 |
| D.乙烯的结构简式CH2CH2 |
设NA为阿伏加德罗常数的数值,下列说法正确的是
| A.1molH2O2中含有的电子数为16NA |
| B.标准状况下,11.2L Br2中含Br—Br键数为0.5NA |
| C.1 mol Fe与足量稀HNO3反应,转移3 NA个电子 |
| D.1 L 0.1 mol ·L-1NaHCO3溶液中含有0.1NA 个HCO3 — |
NA为阿伏加德罗常数的值。下列叙述正确的是
| A.标准状况下,11.2 L H2O中氧原子的数目大于0.5 NA |
| B.6.0 g醋酸晶体中含有H+的数目为0.1 NA |
| C.64gCu粉与足量硫粉加热完全反应生成Cu2S时失去的电子数为2NA |
| D.1 mol Cl-含有的核外电子总数为8 NA |
实验室里需用480 mL 0.10 mol·L-1 CuSO4溶液,现选用500 mL容量瓶进行配制,以下操作正确的是
| A.称取7.68 g硫酸铜,加入500 mL水 |
| B.称取12.0 g胆矾配制500 mL溶液 |
| C.称取8.0 g硫酸铜,加入500 mL水 |
| D.称取12.5 g 胆矾配制500 mL溶液 |
在硫酸铝、硫酸钾和明矾的混合溶液中,如果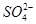 的浓度为0.2 mol·L-1,当加入等体积0.2 mol·L-1KOH溶液时,生成的沉淀恰好完全溶解,(忽略溶液中少量的H+和OH-)则反应后混合溶液中K+的浓度约是
的浓度为0.2 mol·L-1,当加入等体积0.2 mol·L-1KOH溶液时,生成的沉淀恰好完全溶解,(忽略溶液中少量的H+和OH-)则反应后混合溶液中K+的浓度约是
| A.0.125 mol·L-1 | B.0.225 mol·L-1 |
| C.0.250 mol·L-1 | D.0.450 mol·L-1 |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.1 L 0.1 mol·L-1的氨水中含有NH3·H2O分子数为0.1NA |
| B.电解精炼铜时,若阳极质量减少6.4 g,则电路中转移电子数为0.2NA |
| C.标准状况下,2.24 L的二氯甲烷中含有的碳氯共价键的数目为0.2NA |
| D.一定条件下,4.6 g NO2和N2O4混合气体中含有的N原子数目为0.1NA |
某同学用NaHCO3和KHCO3组成的固体混合物进行实验,测得实验数据(盐酸的物质的量浓度相等)如表所示:下列说法不正确的是
| 盐酸/mL | 50 | 50 | 50 |
| 固体混合物质量/g | 9.2 | 15.7 | 27.6 |
| 标准状况下CO2体积/L | 2.24 | 3.36 | 3.36 |
A.盐酸的物质的量浓度为3.0 mol/L
B.根据表中数据能计算出混合物中NaHCO3的质量分数
C.加入9.2 g固体混合物时盐酸过量
D.15.7 g固体混合物恰好与盐酸完全反应