��Ŀ����
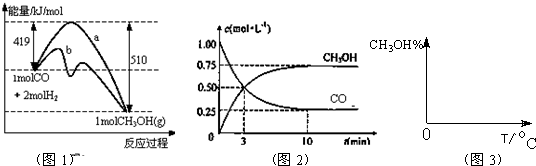
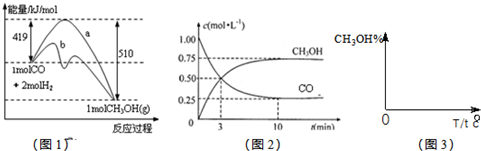
��ҵ����CO����ȼ�ϼ״���һ�������·�����Ӧ��CO(g)+2H2(g) CH3OH(g)��ͼ1��ʾ��Ӧ�������ı仯��ͼ2��ʾһ���¶��£������Ϊ2L���ܱ������м���4mol H2��һ������CO��CO��CH3OH(g)��Ũ����ʱ��仯��
CH3OH(g)��ͼ1��ʾ��Ӧ�������ı仯��ͼ2��ʾһ���¶��£������Ϊ2L���ܱ������м���4mol H2��һ������CO��CO��CH3OH(g)��Ũ����ʱ��仯��
 CH3OH(g)��ͼ1��ʾ��Ӧ�������ı仯��ͼ2��ʾһ���¶��£������Ϊ2L���ܱ������м���4mol H2��һ������CO��CO��CH3OH(g)��Ũ����ʱ��仯��
CH3OH(g)��ͼ1��ʾ��Ӧ�������ı仯��ͼ2��ʾһ���¶��£������Ϊ2L���ܱ������м���4mol H2��һ������CO��CO��CH3OH(g)��Ũ����ʱ��仯��
��1���ڡ�ͼ1���У�����_______���a��b����ʾʹ���˴������÷�Ӧ����_______������ȡ����ȣ���Ӧ��
��2������˵����ȷ����______________
A����ʼ�����COΪ2mol
B������COŨ�ȣ�CO��ת��������
C��������ѹǿ�㶨ʱ����Ӧ�Ѵ�ƽ��״̬
D�������¶Ⱥ��ܱ������ݻ����䣬�ٳ���1molCO��2molH2���ٴδﵽƽ��ʱ n(CH3OH)/n(CO)���С
��3���ӷ�Ӧ��ʼ������ƽ�⣬ v(H2)=________����֪����һ���¶��£���һ�����淴Ӧ�ﵽ��ѧƽ��ʱ��������Ũ����֮���뷴Ӧ��Ũ����֮���ı�ֵ��һ������������������Ǹ÷�Ӧ�Ļ�ѧƽ�ⳣ������ô�ڸ��¶���CO(g)+2H2(g) CH3OH(g)�Ļ�ѧƽ�ⳣ��Ϊ_______________ �������������������䣬����Ӧ��ϵ���£���÷�Ӧ��ѧƽ�ⳣ��____�����������С�����䡱����
CH3OH(g)�Ļ�ѧƽ�ⳣ��Ϊ_______________ �������������������䣬����Ӧ��ϵ���£���÷�Ӧ��ѧƽ�ⳣ��____�����������С�����䡱����
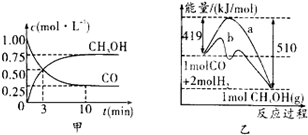
��4�����ڡ�ͼ3���л���ƽ��ʱ�״��ٷֺ����������꣩���¶ȣ������꣩�仯�����ߣ�Ҫ��ѹǿ��ͬ��2�����ߣ��������ϱ��P1��P2����P1<P2����
��5����һ��״����ӽ���Ĥȼ�ϵ�أ��轫�״�����ת��Ϊ���������ַ�Ӧԭ����
A��CH3OH(g)��H2O(g)��CO2(g)��3H2(g) ��H����49.0kJ/mol
B��CH3OH(g)��3/2O2(g)��CO2(g)��2H2O(g) ��H����192.9kJ/mol
��֪H2O(l)= H2O(g) ��H����44 kJ/mol��
��д��32g��CH3OH(g)��ȫȼ������Һ̬ˮ���Ȼ�ѧ����ʽ____________________��
��2������˵����ȷ����______________
A����ʼ�����COΪ2mol
B������COŨ�ȣ�CO��ת��������
C��������ѹǿ�㶨ʱ����Ӧ�Ѵ�ƽ��״̬
D�������¶Ⱥ��ܱ������ݻ����䣬�ٳ���1molCO��2molH2���ٴδﵽƽ��ʱ n(CH3OH)/n(CO)���С
��3���ӷ�Ӧ��ʼ������ƽ�⣬ v(H2)=________����֪����һ���¶��£���һ�����淴Ӧ�ﵽ��ѧƽ��ʱ��������Ũ����֮���뷴Ӧ��Ũ����֮���ı�ֵ��һ������������������Ǹ÷�Ӧ�Ļ�ѧƽ�ⳣ������ô�ڸ��¶���CO(g)+2H2(g)
 CH3OH(g)�Ļ�ѧƽ�ⳣ��Ϊ_______________ �������������������䣬����Ӧ��ϵ���£���÷�Ӧ��ѧƽ�ⳣ��____�����������С�����䡱����
CH3OH(g)�Ļ�ѧƽ�ⳣ��Ϊ_______________ �������������������䣬����Ӧ��ϵ���£���÷�Ӧ��ѧƽ�ⳣ��____�����������С�����䡱������4�����ڡ�ͼ3���л���ƽ��ʱ�״��ٷֺ����������꣩���¶ȣ������꣩�仯�����ߣ�Ҫ��ѹǿ��ͬ��2�����ߣ��������ϱ��P1��P2����P1<P2����
��5����һ��״����ӽ���Ĥȼ�ϵ�أ��轫�״�����ת��Ϊ���������ַ�Ӧԭ����
A��CH3OH(g)��H2O(g)��CO2(g)��3H2(g) ��H����49.0kJ/mol
B��CH3OH(g)��3/2O2(g)��CO2(g)��2H2O(g) ��H����192.9kJ/mol
��֪H2O(l)= H2O(g) ��H����44 kJ/mol��
��д��32g��CH3OH(g)��ȫȼ������Һ̬ˮ���Ȼ�ѧ����ʽ____________________��
��1��b������
��2��AC
��3��0.15mol/L-1��min-1��12 L2��mol-2����С
��4��
��2��AC
��3��0.15mol/L-1��min-1��12 L2��mol-2����С
��4��

��5��CH3OH(g)��3/2O2(g)��CO2(g)��2H2O ��H����280.9kJ/mol

��ϰ��ϵ�д�
 ���Ǽ���С����ϵ�д�
���Ǽ���С����ϵ�д� �Ͻ�ƽ���Ȿϵ�д�
�Ͻ�ƽ���Ȿϵ�д�
�����Ŀ


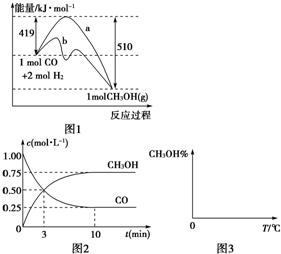 ��ҵ����CO����ȼ�ϼ״���һ�������·�����Ӧ��CO��g��+2H2��g��?CH3OH��g����ͼ1��ʾ��Ӧ�������ı仯��ͼ2��ʾһ���¶��£������Ϊ2L���ܱ������м���4mol H2��һ������CO��CO��CH3OH��g����Ũ����ʱ��仯��
��ҵ����CO����ȼ�ϼ״���һ�������·�����Ӧ��CO��g��+2H2��g��?CH3OH��g����ͼ1��ʾ��Ӧ�������ı仯��ͼ2��ʾһ���¶��£������Ϊ2L���ܱ������м���4mol H2��һ������CO��CO��CH3OH��g����Ũ����ʱ��仯��