题目内容
14.下列关于化学与生产、生活的认识不正确的是( )| A. | 使用清洁能源是防止酸雨发生的重要措施之一 | |
| B. | CO2、CH4、N2等均是造成温室效应的气体 | |
| C. | 节能减排符合低碳经济的要求 | |
| D. | 合理开发利用可燃冰(固态甲烷水合物)有助于缓解能源紧缺 |
分析 A.酸雨主要由化石燃料燃烧产生的二氧化硫、氮氧化物等酸性气体形成的,使用清洁能源减少了二氧化硫、氮氧化物的排放;
B.氮气不能引起温室效应;
C.根据低碳经济的要求判断;
D.开发利用可燃冰为我国在新世纪使用高效新能源开辟了广阔的前景.
解答 解:A.酸雨主要由化石燃料燃烧产生的二氧化硫、氮氧化物等酸性气体形成的,使用清洁能源减少了二氧化硫、氮氧化物的排放,所以使用清洁能源是防止酸雨发生的重要措施之一,故A正确;
B.CO2、CH4等均是造成温室效应的气体,氮气不能引起温室效应,故B错误;
C.节能减排可以减少CO2的排放,符合低碳经济的要求,符合可持续发展战略,故C正确;
D.可燃冰为我国在新世纪使用高效新能源开辟了广阔的前景,合理开发利用可燃冰有助于缓解能源紧缺,故D正确;
故选B.
点评 本题考查环境保护、能源利用问题,是社会关注的焦点问题,熟悉生活中常见的环境污染与治理知识是解题关键,题目难度不大.

练习册系列答案
相关题目
5.检验溶液中是否含有Fe3+可以用的试剂是( )
| A. | 稀HCl | B. | 蔗糖溶液 | C. | KSCN 溶液 | D. | NaCl 溶液 |
19.氯气是氯碱工业的主要产品之一,用作为强氧化剂与氯化剂.下列有关氯气及其化合物的叙述正确的是( )
| A. | 氯气与甲烷发生取代反应,是制取二氯甲烷的有效方法 | |
| B. | 红热的铁丝、铜丝都能在氯气里剧烈燃烧,生成大量白色的烟 | |
| C. | 氯气和次氯酸钠都可用于杀菌、消毒,使用时要注意用量 | |
| D. | 聚氯乙烯是使用量非常大,应用领域最为广泛的塑料,也是熟、热食品常用的包装材料 |
3.钛冶炼厂与氯碱厂、甲醇厂组成一个产业链(如图所示),将大大提高资源的利用率,减少环境污染.
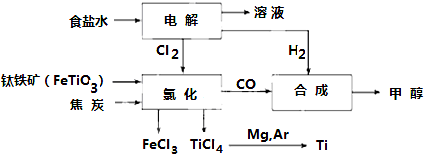
请回答下列问题:
(1)Fe位于元素周期表中第四周期第VIII族.
(2)写出钛铁矿在高温下与焦炭经氯化得到四氯化钛的化学方程式2FeTiO3+6C+7Cl2$\frac{\underline{\;高温\;}}{\;}$2FeCl3+2TiCl4+6CO
(3)制备TiO2的方法之一是利用TiCl4水解生成TiO2•xH2O,再经焙烧制得.写出TiCl4水解的化学方程式:TiCl4+(2+x)H2O=TiO2.xH2O↓+4HCl.
(4)反应后得到Mg、MgCl2、Ti的混合物,可采用蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于1412℃即可.
(5)电解食盐水的离子方程式:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑.

请回答下列问题:
(1)Fe位于元素周期表中第四周期第VIII族.
(2)写出钛铁矿在高温下与焦炭经氯化得到四氯化钛的化学方程式2FeTiO3+6C+7Cl2$\frac{\underline{\;高温\;}}{\;}$2FeCl3+2TiCl4+6CO
(3)制备TiO2的方法之一是利用TiCl4水解生成TiO2•xH2O,再经焙烧制得.写出TiCl4水解的化学方程式:TiCl4+(2+x)H2O=TiO2.xH2O↓+4HCl.
(4)反应后得到Mg、MgCl2、Ti的混合物,可采用蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于1412℃即可.
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
4.X、Y、Z M.N是原子序数依次增大的五种短周期主族元素.其相关信息如下表所示.
(1)M位于元素周期表第四周期ⅥA族,单质M的氧化性比单质Y的氧化性弱(填“强”或“弱”)
(2)X、Z可形成化合物ZX,ZX的电子式为Na+[:H]-(用元素符号表示),ZX与盐酸反应.每生成1molX2时转移电子的物质的量为1mol
(3)实验室中检验N的简单离子的试剂是稀硝酸和硝酸银溶液,反应的离子方程式为Ag++Cl-=AgCl↓
(4)M的氢化物5.6L(标准状况下)完全燃烧生成气态氧化物后恢复到室温,放出的热量为127.6kJ,该条件下反应的热化学方程式为2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H=-510.4kJ/mol.
| 元素 | 相关信息 |
| X | 所有元素中原子半径最小的元素 |
| Y | 地壳中含量最多的元素 |
| Z | 短周期中原子半径最大的金属元素 |
| M | 与Y同主族 |
(2)X、Z可形成化合物ZX,ZX的电子式为Na+[:H]-(用元素符号表示),ZX与盐酸反应.每生成1molX2时转移电子的物质的量为1mol
(3)实验室中检验N的简单离子的试剂是稀硝酸和硝酸银溶液,反应的离子方程式为Ag++Cl-=AgCl↓
(4)M的氢化物5.6L(标准状况下)完全燃烧生成气态氧化物后恢复到室温,放出的热量为127.6kJ,该条件下反应的热化学方程式为2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H=-510.4kJ/mol.
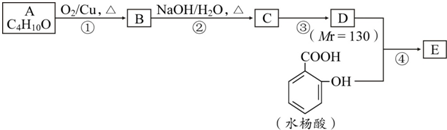

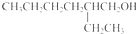 .
.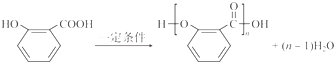 .
.
 晶体的世界丰富多彩,晶体的结构纷繁复杂.人教版课程标准高中教材《选修3》向我们展示了一些典型晶体的结构及性质的相关知识,如:干冰、冰、金刚石、石墨、钋、钾、镁、铜、NaCl、CsCl、CaF2.下图是一个立方晶胞图,请大家在上述所列物质范围内回答下列问题:
晶体的世界丰富多彩,晶体的结构纷繁复杂.人教版课程标准高中教材《选修3》向我们展示了一些典型晶体的结构及性质的相关知识,如:干冰、冰、金刚石、石墨、钋、钾、镁、铜、NaCl、CsCl、CaF2.下图是一个立方晶胞图,请大家在上述所列物质范围内回答下列问题: 已知如图装置的甲、乙两室内装入液体的体积相同.请回答下列问题:
已知如图装置的甲、乙两室内装入液体的体积相同.请回答下列问题: