��Ŀ����
13��ij��ѧʵ��С���ͬѧΪ̽���ͱȽ�SO2����ˮ��Ư���ԣ��������ͼ��ʵ��װ�ã�
��1��ʵ����װ��E���ö������̺�Ũ�����Ʊ�Cl2���÷�Ӧ�Ļ�ѧ����ʽΪ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O������6mol��HCl�μӷ�Ӧ����ת�Ƶĵ��ӵ����ʵ���Ϊ3mol��
��2���ٷ�Ӧ��ʼһ��ʱ��۲쵽B��D�����Թ��е�Ʒ����Һ���ֵ������ǣ�BƷ����Һ��ɫ DƷ����Һ��ɫ��
��ֹͣͨ�����ٽ�B��D�����Թֱܷ���ȣ������Թ��е�������ǣ�B��ɫ��Ʒ���ָֻ��ɺ�ɫ
��3����һ��ʵ��С���ͬѧ��ΪSO2����ˮ����Ư���ԣ�����Ϻ��Ư���Կ϶� ���ǿ�����ǽ��Ƶõ�SO2��Cl2��1��1ͬʱͨ�뵽Ʒ����Һ�У����������ɫЧ��������������������������ӷ���ʽ˵�������������ԭ��Cl2+SO2+2H2O�T4H++2Cl-+SO42-�������ﶼ��Ư���ԣ�
���� ��1�����ݻ��ϼ۱仯����Ŀ��ϻ�ѧ����ʽ��ȷ������ת�Ƶ���Ŀ��
��2�������������ᶼ����Ư���ԣ�������������Ϊ���л�ɫ�ػ������ɲ��ȶ�����ɫ���ʶ�����Ư���ԣ���������Ϊ����ǿ�������ԣ��ܹ����л�ɫ�����������ȶ�����ɫ���ʶ�����Ư���ԣ��ݴ˽��
��3���������н�ǿ�������ԣ�����������н�ǿ�Ļ�ԭ�ԣ���ˮ��Һ�����߷�����ӦCl2+SO2+2H2O�T2HCl+H2SO4���ݴ˽��
��� �⣺��1��ʵ����װ��E���ö������̺�Ũ�����Ʊ�Cl2����Ӧ�Ļ�ѧ����ʽΪ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O����Ӧ��Mn���ϼ���+4�ۡ�+2�ۣ���ÿ��1molMnO2�μӷ�Ӧ������4mol�Ȼ��⣬����1mol������ת��2mol���ӣ�����6mol��HCl�μӷ�Ӧ����ת�Ƶĵ������ʵ���3mol��
�ʴ�Ϊ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��3mol��
��2�������������ᶼ����Ư���ԣ����Թ۲쵽B��D�����Թ��е�Ʒ����Һ���ֵ�������Ʒ����Һ��ɫ��
������������Ϊ���л�ɫ�ػ������ɲ��ȶ�����ɫ���ʶ�����Ư���ԣ���������Ϊ����ǿ�������ԣ��ܹ����л�ɫ�����������ȶ�����ɫ���ʶ�����Ư���ԣ�
���Լ��Ⱥ�B�Թ�������Ϊ����ɫ��Ʒ���ָֻ��ɺ�ɫ��D�Թ�����Ϊ������������
�ʴ�Ϊ��Ʒ����Һ��ɫ��Ʒ����Һ��ɫ����ɫ��Ʒ���ָֻ��ɺ�ɫ��
��3���������н�ǿ�������ԣ�����������н�ǿ�Ļ�ԭ�ԣ���ˮ��Һ������1��1������Ӧ�����ӷ���ʽ��Cl2+SO2+2H2O�T4H++2Cl-+SO42-�������ﶼ��Ư���ԣ����SO2��Cl2��1��1ͬʱͨ�뵽Ʒ����Һʱ��Ʒ����Һ������ɫ��
�ʴ�Ϊ��Cl2+SO2+2H2O�T4H++2Cl-+SO42-�������ﶼ��Ư���ԣ�
���� ���⿼�������Ʊ��Ͷ��������Ư�����ʣ���Ϥ�����Ͷ�������Ư��ԭ���IJ�ͬ�ǽ���ؼ�����Ŀ�Ѷ��еȣ�

 ״Ԫ��ȫ��ͻ�Ƶ�����ϵ�д�
״Ԫ��ȫ��ͻ�Ƶ�����ϵ�д� ֱͨ������У�ܲ��¿�ֱͨ��Уϵ�д�
ֱͨ������У�ܲ��¿�ֱͨ��Уϵ�д� ���й��ڸ��л���������У�����ȷ���ǣ�������
���й��ڸ��л���������У�����ȷ���ǣ�������| A�� | ��������Ʒ�����Ӧ���ų����� | |
| B�� | ���ڴ�����������H2�����ӳɷ�Ӧ | |
| C�� | ��ʹ����KMnO4��Һ��ɫ | |
| D�� | ��ͭ�����������²����ܷ�����������Ӧ |
| A�� | ƽ��������Ӧ�����ƶ��� | B�� | ����B������������С�� | ||
| C�� | ����A��ת���ʼ����� | D�� | a��b |

| A�� | Zn���Ϸ�����ԭ��Ӧ | |
| B�� | ������Zn��a��b��Cu·������ | |
| C�� | Ƭ�̺��ҳ���c��Cu2+����С��c��SO42-���������䣬��Һ���ٱ��ֵ����� | |
| D�� | Ƭ�̺�ɹ۲쵽��ֽa����ɫ |
N2��g��+3H2��g�� $?_{���¸�ѹ}^{����}$2NH3��g����H=-92kJ/mol
��ؼ����������£�
| N��N | H-H | N-H | |
| �������ݣ�KJ/mol�� | 946 | 436 | x |

��1��0-25min�ڣ���Ӧ��ƽ������v��H2��Ϊ0.12mol/��L•min��������x=391��
��2��T��ʱ���÷�Ӧ��ƽ�ⳣ��K=$\frac{4}{27}$L2/mol2���������������
��3��T��ʱ������ʼ����8molN2��24molH2����Ӧ�մﵽƽ��ʱ����ʾc��H2����ͼ����Ӧ�ĵ�ΪB������ĸ����
��4����úΪ��Ҫԭ�ϵĺϳɰ���ҵ�У�ԭ����������������������ã�
��C��s��+H2O��g��?CO��g��+H2��g����H1
��CO��g��+H2O��g��?CO2��g��+H2��g����H2
����֪CO��H2��ȼ���ȷֱ�Ϊ283KJ•mol-1��285.8KJ•mol-1
H2O��g��=H2O��l����H=-44kJ/mol�����H2=-41.2kJ/mol��
��5�������������������Ҫԭ�ϣ��������ͼ1��

д������I�Ļ�ѧ����ʽ��4NH3+5O2$\frac{\underline{����}}{��}$4NO+6H2O
��6��ͼ2�ǿ�ѧ����������õ�ⷨ���³�ѹ���ɵ����������ϳɰ���ʾ��ͼ����ͼ��֪���ѵ缫B�ǵ��ص���������������������������ѵ缫A�ϵĵ缫��ӦʽΪN2+6e-+6H+=2NH3��
| A�� | Ԫ�����ڱ���λ�ڽ����ͷǽ����ֽ��߸�����Ԫ�����ڹ���Ԫ�� | |
| B�� | �����ԭ���У�����˽Ͻ����������˶��ĵ��������ϸ� | |
| C�� | P��S��Cl�õ�������������������Ӧˮ��������Ծ�������ǿ | |
| D�� | Ԫ��ԭ�ӵ���������������Ԫ�ص�����ϼ� |
| A�� | �Ҵ��ķ���ʽ C2H5OH | B�� | �����ӵ�ʵ��ʽΪCH | ||
| C�� | ������ĵ���ʽ 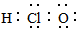 | D�� | ��ϩ�Ľṹ��ʽ CH2CH2 |
| A�� | �ױ�����������ԭ�Ӿ���ͬһ��ƽ���� | |
| B�� | ���ࡢ��֬�������������������¾��ɷ���ˮ�ⷴӦ | |
| C�� | ����ʽΪC3H8O���л�����Ũ���ᡢ���ȵ������·�Ӧ���ܵõ����л�������4�� | |
| D�� | �����������£�CH3CO18OC2H5��ˮ�������CH3CO18OH��C2H5OH |
