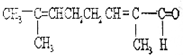题目内容
1.已知二氯化二硫(S2Cl2)的结构式为Cl-S-S-Cl,它易与水反应2S2Cl2+2H2O=4HCl+SO2↑+3S↓.对该反应的说法正确的是( )| A. | S2Cl2既作氧化剂又作还原剂 | |
| B. | H2O作还原剂 | |
| C. | 每生成1molSO2转移4mol电子 | |
| D. | 氧化产物与还原产物物质的量比为3:1 |
分析 2S2Cl2+2H2O=4HCl+SO2↑+3S↓中,S元素的化合价由+1价升高为+4价,S元素的化合价由+1价降低为0,以此来解答.
解答 解:A.只有S元素的化合价变化,则S2Cl2既作氧化剂又作还原剂,故A正确;
B.水中H、O元素的化合价均不变,则水不是还原剂,故B错误;
C.S元素的化合价由+1价升高为+4价,则每生成1molSO2转移3mol电子,故C错误;
D.氧化产物为SO2,还原产物为S,由反应可知二者的物质的量比为1:3,故D错误;
故选A.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
11.在相同条件下,两种气体的物质的量相同,下列说法一定正确的是( )
| A. | 体积均为22.4 L | B. | 具有相同的体积 | ||
| C. | 具有相同的质量 | D. | 具有相同的原子数目 |
12.常温下,下列各组物质不能用一种试剂通过化学反应区别的是( )
| A. | MnO2 CuO FeO | B. | (NH4)2SO4 K2SO4 NH4Cl | ||
| C. | AgNO3 KNO3 Na2CO3 | D. | Na2CO3 NaHCO3 K2CO3 |
9.下列关于新制氯水的叙述不正确的是( )
| A. | 呈黄绿色,说明氯水中有Cl2 | |
| B. | 加入Na2CO3溶液产生气体,说明氯水有酸性 | |
| C. | 加入红色纸条,红色纸条褪色,说明氯水有漂白性 | |
| D. | 滴入石蕊溶液,溶液变成红色并保持不变,说明氯水有酸性 |
16.亚硝酸(HNO2)及其钠盐参加反应时既可作氧化剂又可作还原剂,当它们作还原剂时,生成的含氧化物的可能是( )
| A. | NO | B. | N2 | C. | NO2 | D. | NH3 |
11. 物质X的结构式如图所示,常被用于香料或作为饮料的酸化剂,在食品和医学上用作多价螯合剂,也是化学中间体.下列关于物质X的说法正确的是( )
物质X的结构式如图所示,常被用于香料或作为饮料的酸化剂,在食品和医学上用作多价螯合剂,也是化学中间体.下列关于物质X的说法正确的是( )
 物质X的结构式如图所示,常被用于香料或作为饮料的酸化剂,在食品和医学上用作多价螯合剂,也是化学中间体.下列关于物质X的说法正确的是( )
物质X的结构式如图所示,常被用于香料或作为饮料的酸化剂,在食品和医学上用作多价螯合剂,也是化学中间体.下列关于物质X的说法正确的是( )| A. | X分子式为C6H7O7 | |
| B. | 1 mol物质X可以和3 mol氢气发生加成 | |
| C. | X可以发生消去反应、取代反应等 | |
| D. | 1mol X分别与足量的NaHCO3、Na反应得到的气体体积比为3:2 |
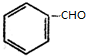 +H2(足量):
+H2(足量):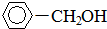 .
.