题目内容
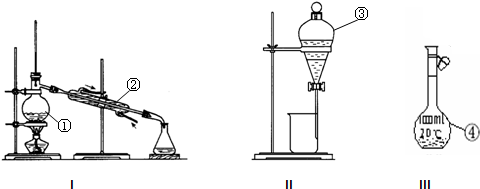
根据下图回答问题:
(1)上述装置中,在反应前用手掌紧贴烧瓶外壁检查装置的气密性,如观察不到明显的现象,还可以用什么简单的方法证明该装置不漏气:___________________________.
(2)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式___________________________.
(3)如果用图中的装置检验上述反应的全部产物,写出下面标号所表示的容器中应加入的试剂的名称及其作用:
A中加入的试剂是__________________,作用是__________________.
B中加入的试剂是__________________,作用是__________________.
C中加入的试剂是__________________,作用是除尽__________________气体.
D中加入的试剂是__________________,作用是__________________.
(4)实验时,C中应观察到的现象是:
答案:
解析:
提示:
解析:
| (1)反应前先用小火加热烧瓶,B、C、D瓶中有气泡冒出,停止加热后,水会升到导管里形成一段水柱,证明装置不漏气
(2) (3)A:无水硫酸铜 检验H2O B:品红溶液 检验SO2 C:酸性KMnO4溶液 SO2 D:澄清石灰水 检验CO2 (4)酸性高锰酸钾溶液的颜色不褪尽(或不褪色,或不褪成无色)
|
提示:
| 中学学过的检查实验装置气密性的方法是:把连接烧瓶的导管的一端浸在水中,用手掌紧贴烧瓶外壁,瓶内空气受热膨胀,如果装置不漏气,导管口会有气泡冒出,手移开,烧瓶冷却水就会升到导管里形成一段水柱.在本题中,由于装置比较大,双手的热量不足以使整个装置中气体膨胀,因而在B、C、D洗气瓶的导管口见不到气泡冒出.如果考生明白检验装置气密性应用的原理,很容易会想到,在反应前用小火加热(或其他方法)使瓶内空气迅速膨胀,导致气泡从洗气瓶的导管中冒出,停止加热后,烧瓶冷却,瓶内压力减小,产生负压,水会升到洗气瓶的导管里,形成一段水柱,由此证明装置不漏气,其道理是一样的.浓H2SO4与木炭粉反应生成H2O(g),SO2(g),CO2(g)三种气态物质,根据中学学过的化学知识,可以用无水硫酸铜检验其中的H2O (g),白色无水CuSO4吸水后变为蓝色CuSO4·5H2O;SO2可以使品红溶液褪色;由于SO2和CO2都能使澄清石灰水变浑浊,所以这里一定要注意,要证明气体中有CO2,先要确认气体中已经不再有SO2.因此在装置中,容器A中的试剂是无水CuSO4、B瓶中是品红溶液、D瓶中是澄清石灰水.由于酸性KMnO4溶液具有强氧化性,而SO2具有还原性,两者可发生氧化还原反应: 因此,C瓶中可加入酸性KMnO4溶液,用来除去剩余的SO2气体.在实验时,C瓶中应观察到的现象是酸性KMnO4溶液的颜色不褪尽.这样才能说明气流中的SO2已经除尽,使澄清石灰水变浑浊只能是由于气体中有SO2.(如果考生回答在C瓶中加人品红溶液,用于检查气流中的SO2是否除尽,且实验时C瓶中品红溶液的颜色不褪尽,也可认为是正确的.)
|

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目