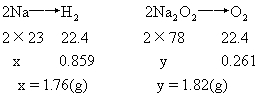题目内容
在一部分被氧化的钠块(氧化部分生成Na2O和Na2O2)5g,与水完全反应,生成气体为1.12L(标准状况),将这些气体引燃后冷却到标准状况,剩余气体为0.336L,求钠块中单质钠、氧化钠、过氧化的各多少克?
答案:
解析:
提示:
解析:
2H2+O2===2H2O ΔV 2 1 3 a b 1.12-0.336=0.784 a=0.523(L) b=0.261(L) 若剩余H2,则H2总体积为:0.523+0.336===0.859(L) O2体积为:0.261(L) Na2O质量:5-1.76-1.82=1.42(g) 若剩余O2,则O2总体积为:0.261+0.336=0.597(L) H2体积:0.523(L) x'=1.07(g) y'=4.16(g) 1.07+4.16>5 不符合题意,舍去。 钠、氧化钠、过氧化钠的质量分别为1.76g、1.42g、1.82g
|
提示:
1.12L气体是H2和O2的混合气体,燃烧后剩作0.336L气体可能是H2,也可能是O2。
|

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目