题目内容
下列各溶液中一定能大量共存的微粒是( )
分析:A.在25℃pH=7的溶液为中性,在80℃pH=1O的溶液,显碱性;
B.常温下c(H+)=10-14mol/L的溶液,显碱性;
C.加入NH4HCO3固体产生气泡的溶液,为酸或碱溶液;
D.离子之间结合生成络离子.
B.常温下c(H+)=10-14mol/L的溶液,显碱性;
C.加入NH4HCO3固体产生气泡的溶液,为酸或碱溶液;
D.离子之间结合生成络离子.
解答:解:A.在25℃pH=7的溶液为中性,在80℃pH=1O的溶液,显碱性,CH3CHO、Ag(NH3)2+发生银镜反应,不能大量共存,故A错误;
B.常温下c(H+)=10-14mol/L的溶液,显碱性,该组离子之间不反应,能大量共存,故B正确;
C.加入NH4HCO3固体产生气泡的溶液,为酸或碱溶液,碱溶液中不能大量存在Mg2+,酸溶液中H+、ClO-、S2-发生氧化还原反应,不能共存,故C错误;
D.Fe3+、SCN-离子之间结合生成络离子,不能大量共存,故D错误;
故选B.
B.常温下c(H+)=10-14mol/L的溶液,显碱性,该组离子之间不反应,能大量共存,故B正确;
C.加入NH4HCO3固体产生气泡的溶液,为酸或碱溶液,碱溶液中不能大量存在Mg2+,酸溶液中H+、ClO-、S2-发生氧化还原反应,不能共存,故C错误;
D.Fe3+、SCN-离子之间结合生成络离子,不能大量共存,故D错误;
故选B.
点评:本题考查离子的共存,为高考常见题型,较好的考查学生思维严密性及分析问题、解决问题的能力,侧重氧化还原反应及复分解反应的考查,信息的抽取及利用为解答的关键,选项AC为解答的难点,题目难度不大.

练习册系列答案
相关题目
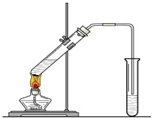 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如右图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如右图所示的装置制取乙酸乙酯.回答下列问题: