题目内容
7.按要求回答下列问题:(1)用浓硫酸给竹筒“刻字”是利用浓硫酸的脱水性.
(2)使品红溶液褪色的气体可以是SO2,也可以是Cl2气体.
(3)在制作印刷电路板的过程中常利用铜与氯化铁溶液反应,该反应的离子方程式是Cu+2Fe3+═Cu2++2Fe2+.
分析 (1)用浓硫酸给竹筒“刻字”是利用浓硫酸的脱水性;
(2)使品红溶液褪色的气体常见Cl2等氧化性气体以及SO2与品红发生化合反应褪色,据此分析解答;
(3)FeCl3溶液与金属铜反应,生成氯化亚铁、氯化铜.
解答 解:(1)用浓硫酸给竹筒“刻字”是利用浓硫酸的脱水性,故答案为:脱水;
(2)Cl2溶于水得到氯水,氯水中H2O+Cl2?HCl+HClO,含有具有漂白性的HClO,也可使品红褪色,故答案为:Cl2;
(3)FeCl3溶液与金属铜反应,生成氯化亚铁、氯化铜,化学反应为2FeCl3+Cu═2FeCl2+CuCl2,所以离子反应方程式为:Cu+2Fe3+═Cu2++2Fe2+,故答案为:Cu+2Fe3+═Cu2++2Fe2+.
点评 本题考查元素化合物的性质,为高频考点,把握浓硫酸的性质、铜的性质及使品红溶液褪色的原理为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
6.化学与社会、科学、技术、环境等有密切联系.下列有关说法正确的是( )
| A. | 用浸泡过酸性高锰酸钾溶液的硅藻土吸收水果产生的乙烯以达到保鲜目的 | |
| B. | PM2.5是指氰、硫的氧化物溶于水形成的酸性液态造成的空气污染 | |
| C. | 新型材料聚酯纤维、光导纤维都属于有机高分子 | |
| D. | 在食品袋长放入盛有硅胶的透气袋,可防止食物氧化变质 |
18.有关苯的下列说法,正确的是( )
| A. | 已烯和苯可用酸性KMnO4溶液来鉴别 | |
| B. | 苯能与氢气发生加成反应,表明苯中含有碳碳双键 | |
| C. | 苯不能使酸性KMnO4溶液褪色,因此苯不能发生氧化反应 | |
| D. | 光照条件下,甲烷与Cl2的反应和苯与Cl2的反应,其反应类型相同 |
15.有4种混合溶液,分别由等体积0.1mol/L的2种溶液混合而成:
①CH3COONa与HCl; ②CH3COONa与NaOH; ③CH3COONa与NaCl;
④CH3COONa与NaHCO3,下列各项排序正确的是( )
①CH3COONa与HCl; ②CH3COONa与NaOH; ③CH3COONa与NaCl;
④CH3COONa与NaHCO3,下列各项排序正确的是( )
| A. | pH:②>③>④>① | B. | c(CH3COO-):②>④>③>① | ||
| C. | 溶液中c(Na+):①>③>②>④ | D. | c(CH3COOH):①>④>③>② |
2.下列化学用语正确的是( )
| A. | 质子数为17、中子数为20的氯原子:${\;}_{17}^{37}$Cl | |
| B. | 氟原子的结构示意图: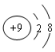 | |
| C. | 明矾的化学式:KAlSO4•12H2O | |
| D. | 次氯酸的电离方程式:HClO=H++ClO- |
12.下列物质溶于水后,溶液能导电,但既不是电解质,又不是非电解质的是( )
| A. | 二氧化硫 | B. | 冰醋酸 | C. | 氧化钙 | D. | 漂白粉 |
19.下列说法不正确的是( )
| A. | 干冰升华和液氯气化时,都只需克服分子间作用力 | |
| B. | 硫酸氢钠晶体溶于水,需要克服离子键和共价键 | |
| C. | 氯化氢气体溶于水时,只有离子键的断裂,没有化学键的形成 | |
| D. | 石墨转化金刚石,既有化学键的断裂,又有化学键的形成 |
16.下列叙述中,正确的是( )
| A. | 二氧化硫溶于水能导电,故二氧化硫是电解质 | |
| B. | 强电解质溶液的导电性一定强于弱电解质溶液的导电性 | |
| C. | 元素从化合态变为游离态,该元素一定被还原 | |
| D. | 发生氧化反应的物质也可能同时发生还原反应 |
12.分类法是学习化学的重要方法,人们在认识事物时可采用多种分类方法.如表(2)中的物质不能与(1)中的物质归为一类的是( )
| 选项 | (1) | (2) |
| A | FeSO4、NO2、MnO2、NaClO、Na2O2 | H2SO3 |
| B | CH3COOH、HOOC-COOH、HClO、H2S | HF |
| C | 复分解反应、电极反应、放热反应、离子反应 | 焰色反应 |
| D | (NH4)2SO4、NH4Cl、NH4NO3、NH3•H2O | NH4HCO3 |
| A. | A | B. | B | C. | C | D. | D |