题目内容
19.写出下列化学方程式和离子方程式㈠NaHSO4溶液中逐滴滴入Ba(OH)2溶液至①恰好中和,溶液呈中性的离子方程式:2H++2OH-+Ba2++SO42-═BaSO4↓+2H2O
②沉淀完全离子方程式:Ba2++SO42-═BaSO4↓
㈡碳酸氢钠NaHCO3溶液与少量的氢氧化钙Ca(OH)2溶液反应,离子方程式:Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O
㈢碳酸氢钠NaHCO3溶液与足量的氢氧化钙Ca(OH)2溶液反应,离子方程式:Ca2++OH-+HCO3-=CaCO3↓+H2O.
分析 ㈠中性时,二者以2:1反应生成硫酸钡、硫酸钠、水;在以上中性溶液中,继续滴加Ba(OH)2溶液,反应生成硫酸钡和水;
㈡少量的氢氧化钙Ca(OH)2溶液完全反应,生成碳酸钙、碳酸钠和水;
㈢碳酸氢钠NaHCO3溶液完全反应,生成碳酸钠、水、NaOH.
解答 解:㈠中性时,二者以2:1反应生成硫酸钡、硫酸钠、水,发生的离子反应为2H++2OH-+Ba2++SO42-═BaSO4↓+2H2O;在以上中性溶液中,继续滴加Ba(OH)2溶液,硫酸根离子沉淀完全,反应生成硫酸钡和水,发生的离子反应为Ba2++SO42-═BaSO4↓,故答案为:2H++2OH-+Ba2++SO42-═BaSO4↓+2H2O;Ba2++SO42-═BaSO4↓;
㈡少量的氢氧化钙Ca(OH)2溶液完全反应,生成碳酸钙、碳酸钠和水,离子反应为Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O,故答案为:Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O;
㈢碳酸氢钠NaHCO3溶液完全反应,生成碳酸钠、水、NaOH,离子反应为Ca2++OH-+HCO3-=CaCO3↓+H2O,故答案为:Ca2++OH-+HCO3-=CaCO3↓+H2O.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重与量有关的离子反应考查,题目难度不大.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
9.汞蒸气有毒,如汞不慎洒在桌面上,应立即洒一些( )
| A. | 硫磺 | B. | 纯碱 | C. | 烧碱 | D. | 细沙 |
7.下列与氯气的氧化性无关的是( )
| A. | 氯气被碱液吸收 | B. | 金属钠在氯气中燃烧 | ||
| C. | 氯气变为液氯 | D. | 氯气溶于水 |
14.将甲、乙两种气体同时通入过量的丙溶液中,可能产生沉淀的组合是( )
| 序号 | 甲 | 乙 | 丙 |
| ① | CO2 | SO2 | Ca(OH)2 |
| ② | HCl | CO2 | Ca(OH)2 |
| ③ | CO2 | SO3 | Ba(NO3)2 |
| ④ | NO2 | SO2 | BaCl2 |
| ⑤ | CO2 | NH3 | CaCl2 |
| ⑥ | O2 | NH3 | MgCl2 |
| A. | ①②⑤ | B. | ①③⑤⑥ | C. | ①②④⑤ | D. | 全部 |
8.下列用电子式表示的形成过程正确的是( )
| A. |  | B. |  | ||
| C. |  | D. |  |
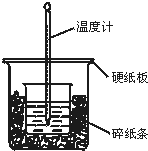 50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:




 $\stackrel{R′OH}{→}$
$\stackrel{R′OH}{→}$ +
+
 +RCl→
+RCl→ +NaCl
+NaCl .
.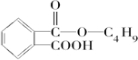 +
+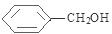 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$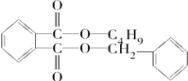 +H2O.
+H2O. .
.