题目内容
19.下列物质中,属于顺式结构的是( )| A. |  | B. |  | C. |  | D. |  |
分析 顺式结构中C=C相连的H原子(或其它相同的基团)在平面的同一侧,据此判断即可.
解答 解:A、 ,相同的原子连在同种原子上,不是顺式结构,故A错误;
,相同的原子连在同种原子上,不是顺式结构,故A错误;
B、 ,只存在一个Cl原子,不存在顺反异构,故B错误;
,只存在一个Cl原子,不存在顺反异构,故B错误;
C、 ,此结构中H或Cl均处于C=C双键的一侧,属于顺式结构,故C正确;
,此结构中H或Cl均处于C=C双键的一侧,属于顺式结构,故C正确;
D、 ,只存在一个Cl原子,另外一个C上连有2个甲基,不存在顺反异构,故D错误,
,只存在一个Cl原子,另外一个C上连有2个甲基,不存在顺反异构,故D错误,
故选C.
点评 本题主要考查的是物质结构的判断,注意顺反异构的定义,难度不大.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
9.“双吸剂”是一种吸收水和氧气的脱氧食品保鲜剂,主要成份为铁粉、碱性粒子(生石灰)、无机盐(氯化钠)、活性炭等.下列有关分析正确的是( )
| A. | “双吸剂”中的无机盐和生石灰都有吸水作用 | |
| B. | “双吸剂”吸收水时,发生了原电池反应 | |
| C. | 吸收氧气的过程中,铁粉作原电池的正极 | |
| D. | 炭粉上发生的反应为:O2+4e-+2H2O=4OH- |
7.下列有机物在常温常压下呈气态的是( )
| A. | 乙烷 | B. | 溴乙烷 | C. | 乙醇 | D. | 乙醛 |
14.下列反应中,可以证明某烃具有不饱和结构的是( )
| A. | 燃烧反应 | B. | 加成反应 | C. | 取代反应 | D. | 裂解反应 |
4.甘氨酸( )和丙氨酸(
)和丙氨酸( )混合,发生缩合反应形成二肽的种类最多为( )
)混合,发生缩合反应形成二肽的种类最多为( )
 )和丙氨酸(
)和丙氨酸( )混合,发生缩合反应形成二肽的种类最多为( )
)混合,发生缩合反应形成二肽的种类最多为( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
8.W,X,Y,Z均为短周期主族元素,原子序数依次增加,且原子核外L电子层的电子数分别为0,6,8,8,它们的最外层电子数之和为10,下列说法正确的是( )
| A. | W与Y可以形成离子化合物 | |
| B. | X的简单氢化物在同主族元素的氢化物中沸点最高,说明X的非金属性最强 | |
| C. | X和Z形成的原子个数1:1的化合物中,既含有极性键又含有非极性键 | |
| D. | 工业生产中,通常用电解Z的熔融氧化物来制取Z的单质 |

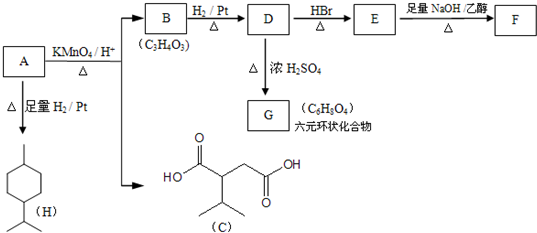
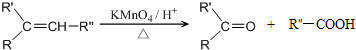
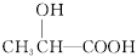 $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$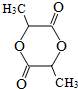 +2H2O.
+2H2O. .
. .
.