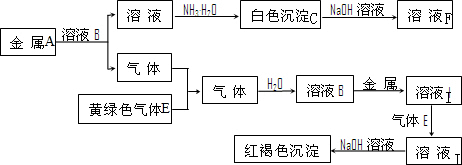
��Ŀ����
��Ҫ��ش�����������1�������ӷ���ʽ���ʹ�����Һȥ�����۵�ԭ��______
��2��д����ĭ������з�Ӧ�����ӷ���ʽ[��Һ��Al2��SO4��3����Һ��NaHCO3]��______
��3��SOCl2��һ��Һ̬������е�Ϊ77�森��ʢ��10mLˮ����ƿ�У�С�ĵμ�8��10��SOCl2���ɹ۲쵽���ҷ�Ӧ��Һ�����а������ɣ�������ɫ�д̼�����ζ�����ݳ����������к���ʹƷ����Һ��ɫ��SO2������ʵ������д��SOCl2��ˮ��Ӧ�Ļ�ѧ����ʽ��____________
����AlCl3��Һ���ܵõ���ˮAlCl3��ʹSOCl2��AlCl3?6H20��ϲ����ȣ��ɵõ���ˮAlCl3������ԭ��______
��4����֪��Ǧ�����ܵĻ�ѧ����ʽΪ��Pb+PbO2+2H2SO4
 2PbSO4+2H2O
2PbSO4+2H2O��Ǧ�����ڷŵ�ʱ������ӦΪ______��
��Ǧ�����ڳ��ʱ������ӦΪ______��
�����Ǧ�����ڷŵ�ʱ��·����2mol����ת��ʱ������H2SO4______mol��
��5�������£����ȡ0.1mol/L HA��Һ��0.1mol/L NaOH��Һ�������ϣ����Ի�Ϻ���Һ����ı仯������û����Һ��pH=8��������Һ��������ʽ�ľ�ȷ����������������֣���
c��OH-��-c��HA��=______ mol/L��
���𰸡���������1��������Һˮ���Լ��ԣ�������Ҫ�ɷ�Ϊ��֬������������ڼ�����Һ��ˮ������������ˮ�����ʣ�
��2����ĭ�������̼�����ƺ���������Һ��ˮ����ٽ��������������Ͷ�����̼���壻
��3�����ݷ�Ӧ�������������Ϊ����������Ȼ������壻SOCl2��ˮ��Ӧ���ɵ��Ȼ������Ȼ���ˮ�����������ã�
��4�������ݵ���ܷ�Ӧ���ŵ���ԭ��أ�Ǧ������ʧ���ӷ���������Ӧ��
�ڳ��ʱԭ��������ӵ�Դ�����������ص�����ʧ���ӷ���������Ӧ��
�����ݵ���ܷ�Ӧ���Ԫ�ػ��ϼ۱仯�������ת�ƽ�ϻ�ѧ����ʽ�������ĵ����
��5��������Һ�������غ�����жϣ�
����⣺��1��������Һˮ���Լ��ԣ�������Ҫ�ɷ�Ϊ��֬������������ڼ�����Һ��ˮ������������ˮ�����ʣ��Լ��Ե����ӷ���ʽΪ��CO32-+H2O?HCO3-+OH-��HCO3-+H2O?H2CO3+OH-
�ʴ�Ϊ��CO32-+H2O?HCO3-+OH-��HCO3-+H2O?H2CO3+OH-��
��2����ĭ�������̼�����ƺ���������Һ��ˮ����ٽ��������������Ͷ�����̼���壻��Ӧ�����ӷ���ʽΪ��3HCO3-+Al3+=Al��OH��3��+3CO2����
�ʴ�Ϊ��3HCO3-+Al3+=Al��OH��3��+3CO2��
��3�����ݷ�Ӧ�������������Ϊ����������Ȼ������壻SOCl2��ˮ��Ӧ���ɵ��Ȼ������Ȼ���ˮ�����������ã���Ӧ�Ļ�ѧ����ʽΪ��SOCl2+H2O=2HCl��+SO2��������AlCl3��Һ���ܵõ���ˮAlCl3��ʹSOCl2��AlCl3?6H20��ϲ����ȣ��ɵõ���ˮAlCl3��SOCl2��ˮ��Ӧ���ɵ��Ȼ������Ȼ���ˮ�����������ã�
�ʴ�Ϊ��SOCl2+H2O=2HCl��+SO2������Ӧ�������Ȼ�����������������ӵ�ˮ�⣻
��4�������ݵ���ܷ�Ӧ���ŵ���ԭ��أ�Ǧ������ʧ���ӷ���������Ӧ���缫��ӦΪ��Pb+SO42--2e-=PbSO4���ʴ�Ϊ��Pb+SO42--2e-=PbSO4��
�ڳ��ʱԭ��������ӵ�Դ�����������ص�������ʧ���ӷ���������Ӧ���缫��ӦΪ��PbSO4+2H2O-2e-=4H++SO42-+PbO2���ʴ�Ϊ��PbSO4+2H2O-2e-=4H++SO42-+PbO2��
��Ǧ�����ܵĻ�ѧ����ʽΪ��Pb+PbO2+2H2SO4 2PbSO4+2H2O�����ݷ�Ӧ��֪����ת��2mol����������2mmol���ʴ�Ϊ��2��
2PbSO4+2H2O�����ݷ�Ӧ��֪����ת��2mol����������2mmol���ʴ�Ϊ��2��
��5��0.1mol/L HA��Һ��0.1mol/L NaOH��Һ������������NaA��Һ����û����Һ��pH=8��c��H+��=10-8mol/L����Һ�Լ��ԣ�˵��A-����ˮ�⣬��Һ�д��������غ㣺c��OH-��=c��H+��+c��HA������c��OH-��-c��HA��=c��H+��=10-8mol/L��
�ʴ�Ϊ��10-8��
���������⿼��������ˮ��ķ���Ӧ�ã�ԭ��ص���ԭ���ķ����жϣ��������Һ�е������غ����Ӧ�ã���Ŀ�Ѷ��еȣ�
��2����ĭ�������̼�����ƺ���������Һ��ˮ����ٽ��������������Ͷ�����̼���壻
��3�����ݷ�Ӧ�������������Ϊ����������Ȼ������壻SOCl2��ˮ��Ӧ���ɵ��Ȼ������Ȼ���ˮ�����������ã�
��4�������ݵ���ܷ�Ӧ���ŵ���ԭ��أ�Ǧ������ʧ���ӷ���������Ӧ��
�ڳ��ʱԭ��������ӵ�Դ�����������ص�����ʧ���ӷ���������Ӧ��
�����ݵ���ܷ�Ӧ���Ԫ�ػ��ϼ۱仯�������ת�ƽ�ϻ�ѧ����ʽ�������ĵ����
��5��������Һ�������غ�����жϣ�
����⣺��1��������Һˮ���Լ��ԣ�������Ҫ�ɷ�Ϊ��֬������������ڼ�����Һ��ˮ������������ˮ�����ʣ��Լ��Ե����ӷ���ʽΪ��CO32-+H2O?HCO3-+OH-��HCO3-+H2O?H2CO3+OH-
�ʴ�Ϊ��CO32-+H2O?HCO3-+OH-��HCO3-+H2O?H2CO3+OH-��
��2����ĭ�������̼�����ƺ���������Һ��ˮ����ٽ��������������Ͷ�����̼���壻��Ӧ�����ӷ���ʽΪ��3HCO3-+Al3+=Al��OH��3��+3CO2����
�ʴ�Ϊ��3HCO3-+Al3+=Al��OH��3��+3CO2��
��3�����ݷ�Ӧ�������������Ϊ����������Ȼ������壻SOCl2��ˮ��Ӧ���ɵ��Ȼ������Ȼ���ˮ�����������ã���Ӧ�Ļ�ѧ����ʽΪ��SOCl2+H2O=2HCl��+SO2��������AlCl3��Һ���ܵõ���ˮAlCl3��ʹSOCl2��AlCl3?6H20��ϲ����ȣ��ɵõ���ˮAlCl3��SOCl2��ˮ��Ӧ���ɵ��Ȼ������Ȼ���ˮ�����������ã�
�ʴ�Ϊ��SOCl2+H2O=2HCl��+SO2������Ӧ�������Ȼ�����������������ӵ�ˮ�⣻
��4�������ݵ���ܷ�Ӧ���ŵ���ԭ��أ�Ǧ������ʧ���ӷ���������Ӧ���缫��ӦΪ��Pb+SO42--2e-=PbSO4���ʴ�Ϊ��Pb+SO42--2e-=PbSO4��
�ڳ��ʱԭ��������ӵ�Դ�����������ص�������ʧ���ӷ���������Ӧ���缫��ӦΪ��PbSO4+2H2O-2e-=4H++SO42-+PbO2���ʴ�Ϊ��PbSO4+2H2O-2e-=4H++SO42-+PbO2��
��Ǧ�����ܵĻ�ѧ����ʽΪ��Pb+PbO2+2H2SO4
 2PbSO4+2H2O�����ݷ�Ӧ��֪����ת��2mol����������2mmol���ʴ�Ϊ��2��
2PbSO4+2H2O�����ݷ�Ӧ��֪����ת��2mol����������2mmol���ʴ�Ϊ��2����5��0.1mol/L HA��Һ��0.1mol/L NaOH��Һ������������NaA��Һ����û����Һ��pH=8��c��H+��=10-8mol/L����Һ�Լ��ԣ�˵��A-����ˮ�⣬��Һ�д��������غ㣺c��OH-��=c��H+��+c��HA������c��OH-��-c��HA��=c��H+��=10-8mol/L��
�ʴ�Ϊ��10-8��
���������⿼��������ˮ��ķ���Ӧ�ã�ԭ��ص���ԭ���ķ����жϣ��������Һ�е������غ����Ӧ�ã���Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
 A��B��C��D�����ɶ�����Ԫ����ɵij������ʣ�����A��B��C����ͬһ��Ԫ�أ���һ���������ת����ϵ��ͼ��ʾ�����ֲ�������ȥ����
A��B��C��D�����ɶ�����Ԫ����ɵij������ʣ�����A��B��C����ͬһ��Ԫ�أ���һ���������ת����ϵ��ͼ��ʾ�����ֲ�������ȥ���� H++CN-��H2O
H++CN-��H2O H++OH-��CN-+H2O
H++OH-��CN-+H2O HCN+OH-
HCN+OH-