题目内容
下列四个试管中,发生如下反应:Zn+2HCl=ZnCl2+H2↑,产生H2的反应速率最小的是( )
| 试管 | 盐酸浓度 | 温度 | 锌的状态 |
| A | 0.5mol·L-1 | 20℃ | 块 状 |
| B | 0.5mol·L-1 | 20℃ | 粉末状 |
| C | 2mol·L-1 | 35℃ | 块 状 |
| D | 2mol·L-1 | 35℃ | 粉末状 |
A
影响化学反应速率的因素有:浓度,反应物的浓度越高反应速率越快;温度,温度越高反应速率越快;压强,有气体反应的增大压强反应速率加快;催化剂,使用催化剂能改变反应速率,一般为加快反应速率;反应物的接触面积越大反应速率越快。。。。所以在上述反应中产生氢气速率最快的为A;

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
 2SO3(g),△H<0。在一定条件下达到平衡状态,时间为t1时改变条件,反应速率与时间关系如图,下列说法正确的是
2SO3(g),△H<0。在一定条件下达到平衡状态,时间为t1时改变条件,反应速率与时间关系如图,下列说法正确的是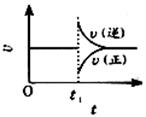
 CO(g)+ H2(g)在一密闭容器中进行,在其它条件不变的情况下,下列条件的改变对其反应速率几乎无影响的是( )
CO(g)+ H2(g)在一密闭容器中进行,在其它条件不变的情况下,下列条件的改变对其反应速率几乎无影响的是( )
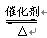 4NO+6H2O。对该反应的有关说法错误的是
4NO+6H2O。对该反应的有关说法错误的是