题目内容
8.用NA表示阿伏加德罗常数的值,下列说法中正确的是( )| A. | 在同温同压时,相同体积的任何气体单质所含的原子数目相同 | |
| B. | 常温常压下,32 g氧气(O2)和32 g臭氧(O3)都含有2NA个氧原子 | |
| C. | 500 mL 0.2 mol/L Na2SO4溶液中含有NA个Na+离子 | |
| D. | 在标准状况下,22.4L水的质量约为18g |
分析 A、气体单质分为单原子分子、双原子分子和多原子分子;
B、氧气和臭氧均由氧原子构成;
C、求出硫酸钠的物质的量,然后根据硫酸钠中含2个钠离子来分析;
D、标况下水为液态.
解答 解:A、同温同压下相同体积的气体单质的物质的量相同,但气体单质分为单原子分子、双原子分子和多原子分子,故含有的原子个数不一定相同,故A错误;
B、氧气和臭氧均由氧原子构成,故32g氧气和32g臭氧中含有的氧原子的物质的量均为2mol,个数均为2NA个,故B正确;
C、溶液中硫酸钠的物质的量n=CV=0.2mol/L×0.5L=0.1mol,而硫酸钠中含2个钠离子,故0.1mol硫酸钠中含0.2mol钠离子即0.2NA个,故C错误;
D、标况下水为液态,故不能根据气体摩尔体积来计算其物质的量,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
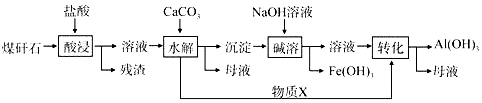
19. 三草酸合铁酸钾晶体(K3[Fe(C2O4)3]•xH2O)是一种光敏材料,110℃时失去全部结晶水.某实验小组为测定该晶体中铁的含量,做了如下实验,完成下列填空:
三草酸合铁酸钾晶体(K3[Fe(C2O4)3]•xH2O)是一种光敏材料,110℃时失去全部结晶水.某实验小组为测定该晶体中铁的含量,做了如下实验,完成下列填空:
步骤一:称取5.0g三草酸合铁酸钾晶体,配制成250mL溶液.
步骤二:取所配溶液25.00mL于锥形瓶中,加H2SO4酸化,滴加KMnO4溶液,发生反应
2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O(Mn2+视为无色).向反应后的溶液中加入锌粉,
加热至黄色刚好消失,过滤并洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时溶
液仍呈酸性.
步骤三:用0.010mol/L KMnO4溶液滴定步骤二所得溶液至终点,滴定中MnO4-被还原成Mn2+.消耗KMnO4溶液体积如下表所示:
(1)步骤一所用仪器已有托盘天平(带砝码)、玻璃棒、烧杯、药匙,还缺少的仪器250mL容量瓶、胶头滴管.
(2)加入锌粉的目的是将Fe3+恰好还原成Fe2+.
(3)写出步骤三中发生反应的离子方程式5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O.
(4)实验测得该晶体中铁元素的质量分数为11.2%.在步骤二中,若滴加的KMnO4溶液的量不够,
则测得铁的含量偏高.(选填“偏低”、“偏高”或“不变”)
 三草酸合铁酸钾晶体(K3[Fe(C2O4)3]•xH2O)是一种光敏材料,110℃时失去全部结晶水.某实验小组为测定该晶体中铁的含量,做了如下实验,完成下列填空:
三草酸合铁酸钾晶体(K3[Fe(C2O4)3]•xH2O)是一种光敏材料,110℃时失去全部结晶水.某实验小组为测定该晶体中铁的含量,做了如下实验,完成下列填空:步骤一:称取5.0g三草酸合铁酸钾晶体,配制成250mL溶液.
步骤二:取所配溶液25.00mL于锥形瓶中,加H2SO4酸化,滴加KMnO4溶液,发生反应
2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O(Mn2+视为无色).向反应后的溶液中加入锌粉,
加热至黄色刚好消失,过滤并洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时溶
液仍呈酸性.
步骤三:用0.010mol/L KMnO4溶液滴定步骤二所得溶液至终点,滴定中MnO4-被还原成Mn2+.消耗KMnO4溶液体积如下表所示:
| 滴定次数 | 滴定起始读数(mL) | 滴定终点读数(mL) |
| 第一次 | 1.08 | 如图 |
| 第二次 | 2.02 | 24.52 |
| 第三次 | 1.00 | 20.98 |
(2)加入锌粉的目的是将Fe3+恰好还原成Fe2+.
(3)写出步骤三中发生反应的离子方程式5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O.
(4)实验测得该晶体中铁元素的质量分数为11.2%.在步骤二中,若滴加的KMnO4溶液的量不够,
则测得铁的含量偏高.(选填“偏低”、“偏高”或“不变”)
16.化学家创造出一种物质“干水”,其每个颗粒含水95%,外层是SiO2,干水吸收二氧化碳的能力比普通清水高三倍.下列有关说法正确的是( )
| A. | 干水和干冰是同一种物质 | |
| B. | 干水是纯净物 | |
| C. | 用干水吸收CO2有助于减缓温室效应 | |
| D. | 干水吸收CO2的过程只发生物理变化 |
3.下列物质不能通过氯气与相应单质直接化合而成的是( )
| A. | NaCl | B. | FeCl2 | C. | HCl | D. | FeCl3 |
13.下列实验操作中正确的是( )
| A. | 蒸馏时,当烧瓶中液体出现暴沸时,要立即添加碎瓷片 | |
| B. | 蒸发操作时,应使溶液蒸发至干,以保证得到的固体中没有任何水分 | |
| C. | 分液操作时,分液漏斗中下层液体先从下口放出,再让上层液体从上口倒出 | |
| D. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
17.化学与生活、生产密切相关.下列食品添加剂中,其使用目的与反应速率有关的是( )
| A. | 调味剂 | B. | 防腐剂 | C. | 增稠剂 | D. | 着色剂 |
10.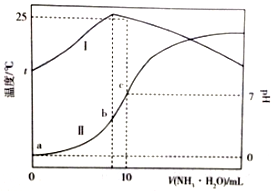 温度为t℃时,在10mL1.0mol/L的盐酸中,逐滴滴入xmol/L的氨水,随着氨水遂渐加入,溶液中的温度变化曲线(曲线I)和pH变化曲线(曲线II)如图所示(忽略混合时溶液体积的变化).下列有关判断正确的是( )
温度为t℃时,在10mL1.0mol/L的盐酸中,逐滴滴入xmol/L的氨水,随着氨水遂渐加入,溶液中的温度变化曲线(曲线I)和pH变化曲线(曲线II)如图所示(忽略混合时溶液体积的变化).下列有关判断正确的是( )
 温度为t℃时,在10mL1.0mol/L的盐酸中,逐滴滴入xmol/L的氨水,随着氨水遂渐加入,溶液中的温度变化曲线(曲线I)和pH变化曲线(曲线II)如图所示(忽略混合时溶液体积的变化).下列有关判断正确的是( )
温度为t℃时,在10mL1.0mol/L的盐酸中,逐滴滴入xmol/L的氨水,随着氨水遂渐加入,溶液中的温度变化曲线(曲线I)和pH变化曲线(曲线II)如图所示(忽略混合时溶液体积的变化).下列有关判断正确的是( )| A. | c点时,c(NH3•H2O)=1.0mol•L-1 | B. | a点时,水的电离程度最大 | ||
| C. | b点时,c(NH4+)>c(Cl-)>c(H+)>c(OH-) | D. | c点时,c(NH3•H2O)=$\frac{x-1}{2}$mol•L-1 |