题目内容
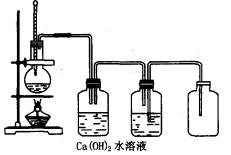
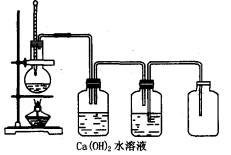
实验室用浓硫酸使乙醇脱水制乙烯,但由于有副反应,致使所生成气体中混有二氧化硫,为了获得纯净的乙烯,某学生设计的实验装置如图。指出其中的错误和缺点,并加以改正。
答案:
解析:
解析:
解题思路:这是一个检查仪器使用和装置原理的带有一定综合性的题目。加热时,除试管外,其他可加热的玻璃仪器均不允许直接用火加热;温度计是测温仪器,它的水银球必须全部接触被测物。洗气装置的进气管末端必须伸进洗涤液中,否则,起不到“洗”的作用;出气导管的进口应在胶塞处。排水收集气体时,进气导管应在胶塞处,排水导管口应接近瓶底,水应装满集气瓶。排出水的导管口,刚伸至盛水的集气瓶口即可。此外,用碱液洗涤酸性气体时,碱液浓度如果太小,则容易很快失效,所以碱溶液浓度大些为佳。 参考答案:错处有五:①未用石棉网。②温度计水银球未伸进液面下。③洗气瓶的进气导管的末端未伸到液面下,出气导管的进口未接近胶塞。④中间集气瓶,应装满水,进气导管口应在胶塞处,排水导管进水口应接近瓶底。⑤排水导管出水口应刚伸至盛水的集气瓶口,否则,停止加热时可能引起水倒吸回集气瓶。缺点是石灰水浓度太小,应该用氢氧化钠溶液。
|

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
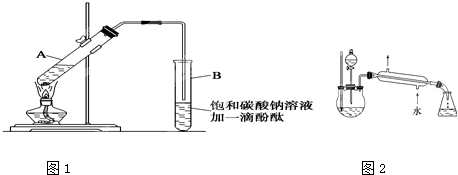
 CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O