题目内容
加热N2O5,依次发生的分解反应为:①N2O5(g)  N2O3(g)+O2(g), ②N2O3(g)
N2O3(g)+O2(g), ②N2O3(g) N2O(g)+O2(g).在容积为2L的密闭容器中充入8mol N2O5,加热到t℃,达到平衡状态后O2为9mol,N2O3为3.4mol.则t℃时反应①的平衡常数为()
N2O(g)+O2(g).在容积为2L的密闭容器中充入8mol N2O5,加热到t℃,达到平衡状态后O2为9mol,N2O3为3.4mol.则t℃时反应①的平衡常数为()
 N2O3(g)+O2(g), ②N2O3(g)
N2O3(g)+O2(g), ②N2O3(g) N2O(g)+O2(g).在容积为2L的密闭容器中充入8mol N2O5,加热到t℃,达到平衡状态后O2为9mol,N2O3为3.4mol.则t℃时反应①的平衡常数为()
N2O(g)+O2(g).在容积为2L的密闭容器中充入8mol N2O5,加热到t℃,达到平衡状态后O2为9mol,N2O3为3.4mol.则t℃时反应①的平衡常数为()| A.10.7 | B.8.5 | C.9.6 | D.10.2 |
B
设反应①中平衡时生成N2O3和氧气都是x,则x-3.4mol+x=9mol,解得x=6.2ml,所以平衡时N2O5的物质的量是8mol-6.2mol=1.8mol,因此t℃时反应①的平衡常数为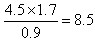 ,答案选B。
,答案选B。
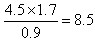 ,答案选B。
,答案选B。
练习册系列答案
相关题目
 2NH3(g) 。下列说法中,表明这一反应已经达到化学平衡状态的是( )
2NH3(g) 。下列说法中,表明这一反应已经达到化学平衡状态的是( )  2NO(g)+O2(g)。达到平衡状态的标志是( )
2NO(g)+O2(g)。达到平衡状态的标志是( ) 2SO3(g),下列操作能增大反应速率并使平衡右移的是( )
2SO3(g),下列操作能增大反应速率并使平衡右移的是( ) CO2(g)+H2 (g)
CO2(g)+H2 (g)
 2C(g)+zD(g),若2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是( )
2C(g)+zD(g),若2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是( )
 2SO3(g) ,此反应放热. 2min 时反应达到化学平衡,此时测得反应物O2还剩余 0.8mol,请填写下列空白:
2SO3(g) ,此反应放热. 2min 时反应达到化学平衡,此时测得反应物O2还剩余 0.8mol,请填写下列空白: