题目内容
(8分) t℃时,将 2molSO2和 1molO2通入体积为 2L 的恒温恒容密闭容器中,发生如下反应:2SO2(g)+O2(g) 2SO3(g) ,此反应放热. 2min 时反应达到化学平衡,此时测得反应物O2还剩余 0.8mol,请填写下列空白:
2SO3(g) ,此反应放热. 2min 时反应达到化学平衡,此时测得反应物O2还剩余 0.8mol,请填写下列空白:
(1)从反应开始到达化学平衡,生成 SO3 的平均反应速率为 ;平衡时,SO2 转化率为 .
(2)下列叙述能证明该反应已达到化学平衡状态的是
A.容器内压强不再发生变化 B.SO2的体积分数不再发生变化
C.容器内气体原子总数不再发生变化 D.相同时间内消耗 2nmolSO2的同时消耗 nmolO2
E.相同时间内消耗 2nmolSO2 的同时生成 nmolO2 F.混合气体密度不再变化
(3)以下操作会引起化学反应速率变快的是
A.向容器中通入O2 B.扩大容器的体积
C.使用正催化剂 D.升高温度 E.向容器中通入氦气
 2SO3(g) ,此反应放热. 2min 时反应达到化学平衡,此时测得反应物O2还剩余 0.8mol,请填写下列空白:
2SO3(g) ,此反应放热. 2min 时反应达到化学平衡,此时测得反应物O2还剩余 0.8mol,请填写下列空白:(1)从反应开始到达化学平衡,生成 SO3 的平均反应速率为 ;平衡时,SO2 转化率为 .
(2)下列叙述能证明该反应已达到化学平衡状态的是
A.容器内压强不再发生变化 B.SO2的体积分数不再发生变化
C.容器内气体原子总数不再发生变化 D.相同时间内消耗 2nmolSO2的同时消耗 nmolO2
E.相同时间内消耗 2nmolSO2 的同时生成 nmolO2 F.混合气体密度不再变化
(3)以下操作会引起化学反应速率变快的是
A.向容器中通入O2 B.扩大容器的体积
C.使用正催化剂 D.升高温度 E.向容器中通入氦气
(8分)(每空1分)
(1) 0.1 mol·(L·s) –1; 20% (2) A B E(3分) (3) A C D(3分)
(1) 0.1 mol·(L·s) –1; 20% (2) A B E(3分) (3) A C D(3分)
2SO2(g) + O2(g)  2SO3(g)
2SO3(g)
初n: 2 1 0
△n: 0.4 0.2 0.4
平n: 1.6 0.8 0.4
(2)C:容器内的原子总数是定值,不能做为平衡判断的标志;D:均为正反应速率,不能做为判断标志;
(3)扩大容器的体积,反应物浓度减小,反应速率降低;恒容下通入氦气,各物质浓度不变,反应速率不变。
 2SO3(g)
2SO3(g)初n: 2 1 0
△n: 0.4 0.2 0.4
平n: 1.6 0.8 0.4
(2)C:容器内的原子总数是定值,不能做为平衡判断的标志;D:均为正反应速率,不能做为判断标志;
(3)扩大容器的体积,反应物浓度减小,反应速率降低;恒容下通入氦气,各物质浓度不变,反应速率不变。

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
 N2O3(g)+O2(g), ②N2O3(g)
N2O3(g)+O2(g), ②N2O3(g) N2O4(g),达到平衡后,再向该容器中充入amol NO2,达到平衡后与原来平衡比较正确的是( )
N2O4(g),达到平衡后,再向该容器中充入amol NO2,达到平衡后与原来平衡比较正确的是( ) B(g),在相同条件下,若分别再向容器中通入一定量的A气体或B气体,重新达到平衡后,容器内A的体积分数比原平衡时
B(g),在相同条件下,若分别再向容器中通入一定量的A气体或B气体,重新达到平衡后,容器内A的体积分数比原平衡时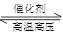 2NH3(反应放热),从反应速率和化学平衡两方面看,合成氨的适宜条件一般为压强:20 MPa—50 MPa,温度:500 ℃左右,催化剂:铁触媒。下列有关合成氨工业的叙述不正确的是
2NH3(反应放热),从反应速率和化学平衡两方面看,合成氨的适宜条件一般为压强:20 MPa—50 MPa,温度:500 ℃左右,催化剂:铁触媒。下列有关合成氨工业的叙述不正确的是 HBr+ HBrO 加入 AgNO3溶液后,溶液颜色变浅
HBr+ HBrO 加入 AgNO3溶液后,溶液颜色变浅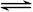 3C(g)+D(s),2分钟反应达到平衡,此时C的浓度为1.2 mol/L。
3C(g)+D(s),2分钟反应达到平衡,此时C的浓度为1.2 mol/L。 CO2(g) +H2(g),达到平衡时测得n(H2)为0.5 mol,下列说法不正确的是( )
CO2(g) +H2(g),达到平衡时测得n(H2)为0.5 mol,下列说法不正确的是( )