题目内容
 (08黄冈中学二模)(15分)已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去)。
(08黄冈中学二模)(15分)已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去)。
(1) 若A和E为单质,组成A单质的元素是自然界中形成化合物种类最多的元素。
① B属于分子 非极性 (填“极性”或“非极性”),B分子中各原子最外层 是 (填“是”或“否”)都满足8电子结构;
② 向50 mL4 mol/L的NaOH溶液中通入1.12 L B(标准状况),
反应后溶液中溶质的物质的量之比为 Na2CO3 :NaOH =1:2 (填化学式和物质的量之比);
③ 4 g A单质完全燃烧放出131.2 kJ的热量,写出表示A单质燃烧热的热化学方程式
C(s)+O2(g)= CO2(g);△H=393.6kJ/mol
(2) 若A为第三周期中的元素所形成的氯化物。
① 写出A溶液→B的离子方程式 Al3++4OH―=AlO2―+2H2O ;
② 写出A和B的溶液反应的离子方程式 Al3++3AlO2―+6H2O=4Al(OH)3↓ 。
(3) 若A为常见的金属,在E的冷、浓溶液中,A有钝化现象。已知:X为含有非极键的离子化合物,且1 mol X含有38 mol电子,向D溶液中加入与D等物质的量的X固体,恰好完全反应,写出该反应的离子方程式 4Fe2++4Na2O2+6H2O=4Fe(OH)3+O2↑+8Na+ 。
答案:(15分) (1) ①非极性 、 是 (4分)
② Na2CO3 :NaOH =1:2 (2分)
③C(s)+O2(g)= CO2(g);△H=393.6kJ/mol (2分)
(2) ①Al3++4OH―=AlO2―+2H2O (2分)
②Al3++3AlO2―+6H2O=4Al(OH)3↓ (2分)
(3) 4Fe2++4Na2O2+6H2O=4Fe(OH)3+O2↑+8Na+ (3分)

 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案2(08浙江省开化中学模拟)实验室中根据2SO2+O2![]() 2SO3;ΔH=-393.2 kJ?mol-1设计如下图所示实验装置来制备SO3固体。请回答下列问题。
2SO3;ΔH=-393.2 kJ?mol-1设计如下图所示实验装置来制备SO3固体。请回答下列问题。
 |
(1)实验前,必须进行的操作是(填操作名称,不必写具体过程)
(2)在A装置中加入Na2SO3固体的同时,还需加几滴水,然后再滴加浓硫酸。加几滴水的作用是
(3)小试管C的作用是
(4)广口瓶D内盛的试剂是 。装置D的三个作用是 ①
② ③
(5)实验中当Cr2O3表面红热时,应将酒精灯移开一会儿再加热,以防温度过高,这样做的原因是
(6)装置F中U型管内收集到的物质的颜色、状态是
(7)装置G的作用是
(8)从G装置导出的尾气处理方法是
(08皖南8校第三次联考)1 L某混合溶液,可能含有的离子如下表:
可能大量还有的阳离子 |
|
可能大量还有的阴离子 |
|
 (1)往该溶液中逐滴加入
(1)往该溶液中逐滴加入![]() 溶液并适当
溶液并适当
加热,产生沉淀和气体的物质的量(![]() )
)
与加入![]() 溶液的体积(V)的关系
溶液的体积(V)的关系
如右图所示。则该溶液中确定含有的离子
有_______________;不能确定是否含有
的阳离子有______________,要确定其存
在可补充做的实验是___________;肯定不存在的阴离子有_________________。
(2)经检测,该溶液中含有大量的![]() ,若向1 L该混合溶液中通入―定晕的
,若向1 L该混合溶液中通入―定晕的![]() ,溶液中
,溶液中![]() 的物质的量与通入
的物质的量与通入![]() 的体积(标准状况)的关系如下表所示,分析后回答下列问题:
的体积(标准状况)的关系如下表所示,分析后回答下列问题:

 (08安徽信息卷)2008年北京奥运会体现“人文奥运”的一个重要举措是坚决反对运动员服用兴奋剂。利尿酸足一种被禁止使用的药物,其结构简式如图所示。下列有关利尿酸说法正确的是()
(08安徽信息卷)2008年北京奥运会体现“人文奥运”的一个重要举措是坚决反对运动员服用兴奋剂。利尿酸足一种被禁止使用的药物,其结构简式如图所示。下列有关利尿酸说法正确的是()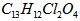
 溶液发生显色反应
溶液发生显色反应 。下列说法正确的是()
。下列说法正确的是() A.a极为电池的正极
A.a极为电池的正极
 厍仑的电量
厍仑的电量  ①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H1=+49.0KJ/mol
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H1=+49.0KJ/mol