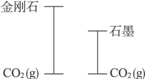题目内容
|
1955年,美国通用电气公司专门制造了高温高压静电设备,得到世界上第一批工业用人造金刚石小晶体,从而开创了工业规模生产人造金刚石磨料的先河,现在他们的年产量在20吨左右.不久,杜邦公司发明了爆炸法,利用瞬时爆炸产生的高压和急剧升温,也获得了几毫米大小的人造金刚石. 已知25℃、101 kPa下,石墨、金刚石燃烧的热化学方程式分别为 C(石墨,s)+O2(g) C(金刚石,s)+O2(g)=CO2(g) ΔH=-395.41 kJ·mol-1 据此判断,下列说法正确的是 | |
| [ ] | |
A. |
由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的低 |
B. |
由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的高 |
C. |
由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的低 |
D. |
由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的高 |
答案:A
解析:
解析:
|
思路解析:本题考查反应热、燃烧热的概念以及物质所含能量的高低与稳定性的关系. 经过反应,金刚石和石墨都生成了CO2,终点相同. 方法1:两式相减可得C(石墨,s) 方法2(画图法):由放热数据知,在终点相同的情况下,金刚石放热多,则金刚石的起点高,能量高,如下图所示:
所以石墨转变成金刚石需要吸热.金刚石的能量更高,石墨的能量更低.此外,通过研究转化条件,我们可以让反应向我们需要的方向进行. 绿色通道:判断反应是吸热还是放热,可以通过热化学方程式相加减来进行;用画图法可以直观地理解和判断能量的高低.物质的能量越低,该物质越稳定.例如,由该题可知石墨比金刚石能量低,更稳定. |

练习册系列答案
 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案
相关题目