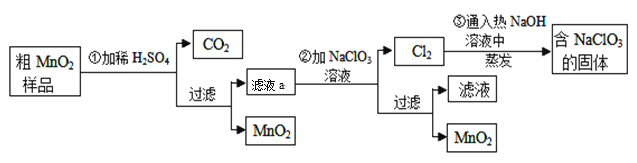
题目内容
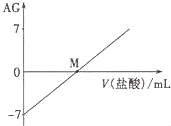
【题目】溶液的酸碱性可用酸度(AG)表示,已知AG =lg![]() ,室温下将0.01molL﹣l盐酸逐滴滴入20.00mL 0.01 molL﹣l氨水中,溶液的AG变化如图所示,下列说法正确的是
,室温下将0.01molL﹣l盐酸逐滴滴入20.00mL 0.01 molL﹣l氨水中,溶液的AG变化如图所示,下列说法正确的是
A.室温下,0.01 molL﹣l盐酸的AG=12
B.M点时溶液中:c(NH4+)=c(Cl﹣)
C.M点加入盐酸的体积大于20.00 mL
D.M点以后NH4+的水解程度逐渐增大
【答案】B
【解析】
试题分析:A.室温下,0.01 molL-l盐酸中氢离子浓度为0.01mol/L,氢氧根离子浓度为10-12mol/L,该盐酸的AG=![]() =lg10,故A错误;B.根据图象可知,M点的AG=lg
=lg10,故A错误;B.根据图象可知,M点的AG=lg![]() =0,则c(H+)=c(OH-),根据电荷守恒可知c(NH4+)=c(Cl-),故B正确;C.M点时c(H+)=c(OH-),溶液呈中性,当加入盐酸的体积为20.00 mL时,溶质为氯化铵,溶液为酸性,若为中性,则加入盐酸体积稍小于20.00mL,故C错误;D.M点后,若盐酸过量,HCl电离出的氢离子抑制了铵根离子的水解,故D错误;故选B。
=0,则c(H+)=c(OH-),根据电荷守恒可知c(NH4+)=c(Cl-),故B正确;C.M点时c(H+)=c(OH-),溶液呈中性,当加入盐酸的体积为20.00 mL时,溶质为氯化铵,溶液为酸性,若为中性,则加入盐酸体积稍小于20.00mL,故C错误;D.M点后,若盐酸过量,HCl电离出的氢离子抑制了铵根离子的水解,故D错误;故选B。

 阅读快车系列答案
阅读快车系列答案【题目】下列有关反应热的叙述中正确的是
①已知2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ·mol-1,则氢气的燃烧热为△H=-241.8kJ·mol-1
②由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
③X(g)+Y(g)![]() Z(g)+W(s) △H>0,恒温恒容条件下达到平衡后加入X,上述反应的△H增大
Z(g)+W(s) △H>0,恒温恒容条件下达到平衡后加入X,上述反应的△H增大
④已知:
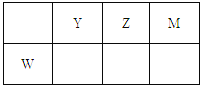
共价键 | C—C | C=C | C—H | H—H |
键能/(kJ·mol-1) | 348 | 610 | 413 | 436 |
上表数据可以计算出 的焓变
的焓变
⑤根据盖斯定律,推知在相同条件下,金刚石或石墨燃烧生成1molCO2固体时,放出的热量相等
⑥25℃,101kPa,1mol碳完全燃烧生成CO2所放出的热量为碳的燃烧热
A.①②③④ B.③④⑤ C.④⑤ D.⑥