题目内容
硝化甘油(C3H5N3O9)分解时产物为N2、CO2、O2和H2O,它分解的反应方程式为________.已知20℃时,2.27 g硝化甘油分解放出热量15.4 kJ,则每生成1 mol常温下气体放出的热量为________kJ.
答案:
解析:
解析:
答案:4C3H5N3O9![]() 6N2↑+12CO2↑+O2↑+10H2O 324 kJ
6N2↑+12CO2↑+O2↑+10H2O 324 kJ
解:由产物书写方程式
4C3H5N3O9![]() 6N2↑+12CO2↑+O2↑+10H2O
6N2↑+12CO2↑+O2↑+10H2O
20℃时生成1 mol气体需C3H5N3O9为![]() mol.C3H5N3O9的相对分子质量为227.故需要的质量为
mol.C3H5N3O9的相对分子质量为227.故需要的质量为![]() ×227 g.列出比例式
×227 g.列出比例式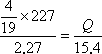
解得Q=324(kJ)

练习册系列答案
相关题目
以下不属于酯类物质的是( )
| A、甘氨酸 | B、硝化甘油 | C、脂肪 | D、硝酸纤维 |