题目内容
下列有关原子结构和元素周期律的表述正确的是 ( )
①原子序数为15的元素的最高化合价为+3 ②ⅦA族元素是同周期中非金属性最强的元素 ③第二周期ⅣA族元素的原子核电荷数和中子数一定为6 ④原子序数为12的元素位于元素周期表的第三周期ⅡA族
| A.①② | B.①③ | C.②④ | D.③④ |
C
解析试题分析:①原子序数为15的元素磷元素,位于VA族,最高化合价为+5,错误; ②ⅦA族元素是同周期中非金属性最强的元素,正确;③第二周期ⅣA族元素碳元素的原子核电荷数和电子数一定为6,中子数不一定为6,错误; ④原子序数为12的元素镁元素位于元素周期表的第三周期ⅡA族,正确,选C。
考点:考查常见元素在周期表中的位置和性质。

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案四种短周期元素在周期表中的位置如图,其中只有M为金属元素。下列说法不正确的是( ) 
| | Y | Z | |
| M | X | | |
B.Y的最高价氧化物对应水化物的酸性比X 的弱
C.X 的最简单气态氢化物的热稳定性比Z的小
D.Z位于元素周期表中第2 周期、第ⅥA族
四种主族元素的离子a Xm+,bYn+,cZn-和dRm-(a,b,c,d为元素的原子序数),它们具有相同的电子层结构,若m>n,对下列叙述的判断正确的是( )
①a-b=n-m ②元素的原子序数a>b>c>d
③元素非金属性Z>R ④最高价氧化物对应水化物碱性X>Y
| A.②③正确 | B.只有③正确 | C.①②③④正确 | D.①②③正确 |
阴离子 含中子N个,X的质量数为A,a g X的氢化物中含质子的物质的量是( )
含中子N个,X的质量数为A,a g X的氢化物中含质子的物质的量是( )
A. mol mol | B. mol mol |
C. mol mol | D. mol mol |
两种微粒含有相同的质子数和电子数,这两种微粒的关系可能是:(1)同一元素的不同原子,(2)不同元素的原子,(3)两种不同的分子,(4)一种原子和一种分子,(5)一种原子和一种离子,(6)一种分子和一种离子,(7)两种不同的阳离子,(8)两种不同的阴离子,(9)一种阴离子和一种阳离子,其中正确的是
| A.(1)(3)(4)(7)(8) | B.(1)(2)(5)(7)(9) |
| C.(1)(2)(5)(7)(9) | D.(1)(2)(3)(4)(5) |
天然存在的金属钫(Fr)极微量。它的21种已知同位素都有放射性。它是碱金属元素中最重的元素。根据它在周期表中的位置预言其性质,其中不正确的是( )
| A.在空气中燃烧时生成氧化物Fr2O | B.在已知元素中具有最大的原子半径 |
| C.氧化物对应的水化物碱性极强 | D.其单质的熔点比金属钠的熔点低 |
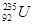 是重要的核工业原料,但在自然界的丰度很低,
是重要的核工业原料,但在自然界的丰度很低,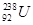 互为同位素
互为同位素