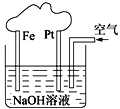
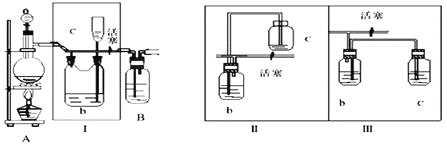
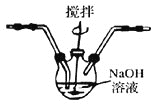
题目内容
【题目】设NA代表阿伏加德罗常数的值,下列叙述正确的是( )
A. 46g组成为C2H6O的有机物,C—H键数目一定为5NA
B. 1mol羟基中含有的电子数为10NA
C. 标准状况下,1mol CCl4的体积约为22.4 L
D. 14g乙烯和丙烯的混合气体中所含原子总数为3NA
【答案】D
【解析】试题分析:A、依据n=![]() 计算物质的量=
计算物质的量=![]() =1mol,有机物C2H6O存在同分异构体,若为乙醇含有极性键的数目一定为7NA,若为甲醚含有极性键的数目一定为8NA,故A错误;B、羟基的电子式为:
=1mol,有机物C2H6O存在同分异构体,若为乙醇含有极性键的数目一定为7NA,若为甲醚含有极性键的数目一定为8NA,故A错误;B、羟基的电子式为:![]() ,1mol羟基中含有9mol电子,故B错误;C、标准状况下,CCl4是液体,1mol CCl4的体积小于22.4 L,故C错误;D、14g乙烯、丙烯的混合气体中含有1mol最简式CH2,含有3mol原子,含有的原子数为3 NA,故D正确;故选D。
,1mol羟基中含有9mol电子,故B错误;C、标准状况下,CCl4是液体,1mol CCl4的体积小于22.4 L,故C错误;D、14g乙烯、丙烯的混合气体中含有1mol最简式CH2,含有3mol原子,含有的原子数为3 NA,故D正确;故选D。

【题目】四氯化锡![]() 是一种重要的化工产品。某兴趣小组拟制备四氯化锡。
是一种重要的化工产品。某兴趣小组拟制备四氯化锡。
I.(查阅资料)
物质 | 熔点 | 沸点 | 化学性质 |
Sn | 231 | 227 | 加热时与 |
| 246 | 652 |
|
|
| 114 | 极易水解 |
Ⅱ![]() (制备产品)
(制备产品)
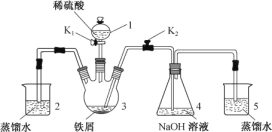
实验装置如图所示![]() 省略夹持和加热装置
省略夹持和加热装置![]()
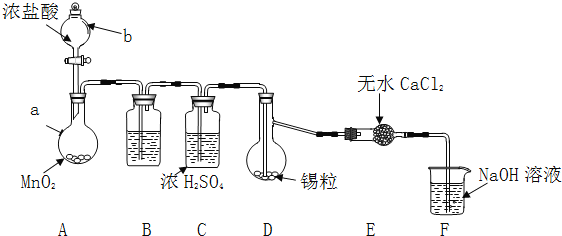
实验步骤:
(1)检查装置气密性后,按图示加入试剂.仪器b的名称是 ______ ,其中无水![]() 的作用是 ______ ,B中的试剂是 ______
的作用是 ______ ,B中的试剂是 ______ ![]() 选填下列字母编号
选填下列字母编号![]() 。
。
A.![]() 溶液
溶液 ![]() 溶液
溶液
![]() 饱和NaCl溶液
饱和NaCl溶液 ![]() 溶液
溶液
(2)先向A中烧瓶内加入盐酸并加热a,当整个装置 ______ 后![]() 填实验现象
填实验现象![]() ,再加热熔化锡粒,反应完后,停止加热。
,再加热熔化锡粒,反应完后,停止加热。
(3)待反应结束后,经 ______ ![]() 填写操作名称
填写操作名称![]() 、洗涤、干燥,可回收利用装置A中未反应完的
、洗涤、干燥,可回收利用装置A中未反应完的![]() 。
。
Ⅲ![]() 探究与反思
探究与反思![]()
(1)装置F中吸收![]() 发生反应的离子方程式是 ______ 。
发生反应的离子方程式是 ______ 。
(2)实验在D中得到的产品很少,经分析装置设计有缺陷,应在D和E之间补充 ______ ![]() 填装置名称
填装置名称![]() 。
。
(3)为验证产品中是否含有![]() ,该小组设计了以下实验方案:
,该小组设计了以下实验方案:![]() 所需试剂从稀
所需试剂从稀![]() 、稀HCl、
、稀HCl、![]() 溶液、
溶液、![]() 溶液、KSCN溶液、蒸馏水中选择
溶液、KSCN溶液、蒸馏水中选择![]()
取适量![]() 产品溶入20mL蒸馏水中,加入 ______ ,若 ______
产品溶入20mL蒸馏水中,加入 ______ ,若 ______ ![]() 填实验现象
填实验现象![]() ,则含有
,则含有![]() ,否则无
,否则无![]() 。
。