题目内容
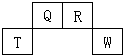 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族族序数相等,请回答下列问题:
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族族序数相等,请回答下列问题:(1)T元素的原子结构示意图为
第二周期ⅣA族
第二周期ⅣA族
,R元素单质的电子式为

(2)原子序数比T少2的元素是
Na
Na
(填元素符号),用电子式表示该元素与W元素形成化合物的过程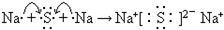
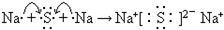
(3)原子序数比W多4的元素是
Ca
Ca
(填元素符号),该元素最高价氧化物的水化物溶液与W元素最高价氧化物的水化物溶液反应的离子方程式为:Ca2++2OH-+2H++SO42-=CaSO4↓+2H2O
Ca2++2OH-+2H++SO42-=CaSO4↓+2H2O
.分析:(1)根据元素的原子结构知识来来确定原子核外电子排布以及在周期表的位置;
(2)硫化钠是含有离子键的离子化合物;
(3)氢氧化钙是强碱,硫酸是强酸,二者之间发生中和反应生成硫酸钙和水.
(2)硫化钠是含有离子键的离子化合物;
(3)氢氧化钙是强碱,硫酸是强酸,二者之间发生中和反应生成硫酸钙和水.
解答:解:图中所示是短周期元素Q、R、T、W在元素周期表中的位置,因为T所处的周期序数与主族族序数相等,所以可以知道T是Al,Q是C,R是N,W是S.
(1)铝元素的原子结构示意图为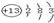 ,C在周期表中的位置是第二周期ⅣA族,氮气是含有氮氮叁键的物质,电子式为:
,C在周期表中的位置是第二周期ⅣA族,氮气是含有氮氮叁键的物质,电子式为: ,故答案为:
,故答案为: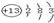 ;第二周期ⅣA族;
;第二周期ⅣA族; ;
;
(2)原子序数比Al少2的元素是Na,硫化钠是硫元素和钠元素之间通过离子键形成的离子化合物,形成过程表示为: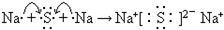 ,故答案为:Na;
,故答案为:Na;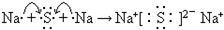 ;
;
(3)原子序数比S多4的元素是Ca,该元素最高价氧化物的水化物是氢氧化钙,S元素最高价氧化物的水化物是硫酸,氢氧化钙是强碱,硫酸是强酸,二者之间发生中和反应生成硫酸钙和水,实质是:Ca2++2OH-+2H++SO42-=CaSO4↓+2H2O,故答案为:Ca;Ca2++2OH-+2H++SO42-=CaSO4↓+2H2O.
(1)铝元素的原子结构示意图为
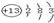 ,C在周期表中的位置是第二周期ⅣA族,氮气是含有氮氮叁键的物质,电子式为:
,C在周期表中的位置是第二周期ⅣA族,氮气是含有氮氮叁键的物质,电子式为: ,故答案为:
,故答案为: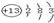 ;第二周期ⅣA族;
;第二周期ⅣA族; ;
;(2)原子序数比Al少2的元素是Na,硫化钠是硫元素和钠元素之间通过离子键形成的离子化合物,形成过程表示为:
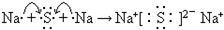 ,故答案为:Na;
,故答案为:Na;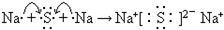 ;
;(3)原子序数比S多4的元素是Ca,该元素最高价氧化物的水化物是氢氧化钙,S元素最高价氧化物的水化物是硫酸,氢氧化钙是强碱,硫酸是强酸,二者之间发生中和反应生成硫酸钙和水,实质是:Ca2++2OH-+2H++SO42-=CaSO4↓+2H2O,故答案为:Ca;Ca2++2OH-+2H++SO42-=CaSO4↓+2H2O.
点评:本题考查学生元素周期表和元素周期律知识,可以根据所学知识进行回答,难度不大.

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
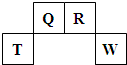 (2009?福建)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等.
(2009?福建)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等.
 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,
 短周期元素Q、R、T、W在元素周期表中的位置如右图所示,期中元素T所处的周期序数与主族序数相等,请回答下列问题:
短周期元素Q、R、T、W在元素周期表中的位置如右图所示,期中元素T所处的周期序数与主族序数相等,请回答下列问题:
 (2013?番禺区模拟)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,下列推断正确的是( )
(2013?番禺区模拟)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,下列推断正确的是( )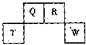 (2012?长宁区一模)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:
(2012?长宁区一模)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题: