题目内容
(1)一个典型病毒微粒的直径是5×10-6cm,如果把阿伏加德罗常数个这种病毒排成一行,其长度是______cm.
(2)19g某二价金属氯化物ACl2中含有0.4molCl-,则ACl2的摩尔质量是______;A的相对原子质量是______;ACl2的化学式是______.
解:(1)长度为:5×10-6cm×6.02×1023=3.01×1018cm,故答案为:3.01×1018;
(2)n(ACl2)= n(Cl-)=0.2mol,M(ACl2)=
n(Cl-)=0.2mol,M(ACl2)=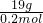 =95g/mol,
=95g/mol,
A的相对原子质量是95-2×35.5=24,为Mg元素,ACl2的化学式是MgCl2,
故答案为:95g/mol;24;MgCl2.
分析:(1)根据总长度等于粒子个数乘以粒子直径计算;
(2)n= 结合氯化物的组成分析.
结合氯化物的组成分析.
点评:本题考查阿伏加德罗常数、摩尔质量以及相对原子质量的计算,题目难度不大,注意有关计算公式的运用.
(2)n(ACl2)=
 n(Cl-)=0.2mol,M(ACl2)=
n(Cl-)=0.2mol,M(ACl2)=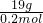 =95g/mol,
=95g/mol,A的相对原子质量是95-2×35.5=24,为Mg元素,ACl2的化学式是MgCl2,
故答案为:95g/mol;24;MgCl2.
分析:(1)根据总长度等于粒子个数乘以粒子直径计算;
(2)n=
 结合氯化物的组成分析.
结合氯化物的组成分析.点评:本题考查阿伏加德罗常数、摩尔质量以及相对原子质量的计算,题目难度不大,注意有关计算公式的运用.

练习册系列答案
 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目