题目内容
2.铅蓄电池的两极分别为Pb、PbO2,电解质溶液为硫酸,工作时反应为:Pb+PbO2+2H2SO4═2PbSO4+2H2O下列结论正确的是( )| A. | Pb为正极被氧化 | B. | SO42-只向PbO2极移动 | ||
| C. | 电解质溶液密度不断减小 | D. | 电解质溶液浓度不变 |
分析 由铅蓄电池的总反应PbO2+2H2SO4+Pb═2PbSO4+2H2O可知,放电时,Pb被氧化,应为电池负极反应,
电极反应式为Pb-2e-+SO42-=PbSO4,正极上PbO2得电子被还原,电极反应式为PbO2+SO42-+2e-+4H+═PbSO4+2H2O,原电池中阳离子向正极移动,阴离子向负极移动.
解答 解:A.由铅蓄电池的总反应PbO2+2H2SO4+Pb═2PbSO4+2H2O可知,Pb为负极,发生失电子的氧化反应,被氧化,故A错误;
B、原电池中阳离子向正极移动,阴离子硫酸根向负极Pb极移动,故B错误;
C、由铅蓄电池的总反应PbO2+2H2SO4+Pb═2PbSO4+2H2O可知,硫酸被消耗,所以电解质溶液密度不断减小,故C正确;
D、由铅蓄电池的总反应PbO2+2H2SO4+Pb═2PbSO4+2H2O可知,硫酸被消耗,电解质的浓度减小,故D错误;
故选C.
点评 本题考查原电池的工作原理,题目难度中等,本题注意电极反应式的书写,为解答该题的关键.

练习册系列答案
相关题目
9.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 0.1mol•L-1 FeCl3溶液:K+、NH${\;}_{4}^{+}$、I-、SCN- | |
| B. | 使甲基橙试液呈红色的溶液:K+、Na+、SO${\;}_{4}^{2-}$、AlO${\;}_{2}^{-}$ | |
| C. | $\frac{{K}_{w}}{c({H}^{+})}$=1×10-13 mol•L-1的溶液中:Al3+、Ca2+、Cl-、NO${\;}_{3}^{-}$ | |
| D. | 水电离产生的c(OH-)=10-12 mol•L-1的溶液:NH${\;}_{4}^{+}$、Mg2+、HCO${\;}_{3}^{-}$、Cl- |
13.下列关于化石燃料的加工说法不正确的是( )
| A. | 石油裂解主要得到乙烯 | |
| B. | 煤干馏主要得到焦炭、煤焦油、粗氨水和焦炉气 | |
| C. | 石蜡油受热分解产生了可以使酸性高锰酸钾溶液褪色的烯烃 | |
| D. | 煤制煤气是物理变化,是高效、清洁地利用煤的重要途径 |
10.下列各组物质在一定条件下反应,可以制得较纯净的1,2-二氯乙烷的是( )
| A. | 乙烷与氯气混合 | B. | 乙烯与氯气混合 | ||
| C. | 乙烯与氯化氢气体混合 | D. | 乙烯通入浓盐酸 |
7.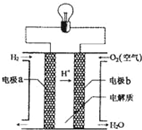 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法正确的是( )
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法正确的是( )
 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法正确的是( )
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法正确的是( )| A. | 该电池工作时电能转化为化学能 | |
| B. | 该电池中电极a是正极 | |
| C. | 外电路中电子由电极a通过导线流向电极b | |
| D. | 该电池的总反应:H2+O2═H2O |
11.火力发电是通过化石燃料燃烧,使化石燃料中化学能转化为电能,其能量转化方式正确的是( )
| A. | 化学能$\stackrel{△}{→}$电能 | B. | 化学能$\stackrel{△}{→}$机械能$\stackrel{△}{→}$电能 | ||
| C. | 化学能$\stackrel{△}{→}$热能$\stackrel{△}{→}$电能 | D. | 化学能$\stackrel{△}{→}$热能$\stackrel{△}{→}$机械能$\stackrel{△}{→}$电能 |
12.下列设备工作时能将电能转化为化学能的是( )
| A. |  硅太阳能电池 | B. |  钠冶炼槽 | C. |  太阳能集热器 | D. |  氢氧燃料电池 |
 不同价态锰的微粒的能量(△G)如图.若某种含锰微粒(如Mn3+)的能量处于相邻价态两种微粒(Mn2+和MnO2)能量连线左上方,则该微粒不稳定并发生歧化反应,转化为相邻价态的微粒.
不同价态锰的微粒的能量(△G)如图.若某种含锰微粒(如Mn3+)的能量处于相邻价态两种微粒(Mn2+和MnO2)能量连线左上方,则该微粒不稳定并发生歧化反应,转化为相邻价态的微粒.