题目内容
【题目】下列事实不能用勒夏特列原理解释的是( )
A.光照新制的氯水时,溶液的pH逐渐减小
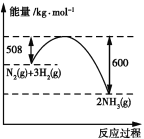
B.高温,使N2和H2转化为更多的NH3(△H<0)
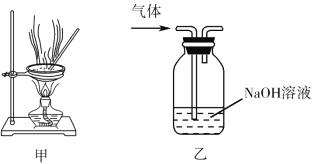
C.可用浓氨水和氢氧化钠固体快速制取氨气
D.增大压强,有利于SO2和O2反应生成SO3
【答案】B
【解析】
A. 氯水中存在化学平衡Cl2+H2O ![]() HCl+HClO,光照使氯水中的次氯酸分解,次氯酸浓度减小,使得平衡向右移动,氢离子浓度变大,溶液的pH值减小,能用勒夏特列原理解释,故A不符合;
HCl+HClO,光照使氯水中的次氯酸分解,次氯酸浓度减小,使得平衡向右移动,氢离子浓度变大,溶液的pH值减小,能用勒夏特列原理解释,故A不符合;
B. N2和H2转化为NH3的反应△H<0,是放热反应,升高温度反应逆向移动,不能使N2和H2转化为更多的NH3,不能用勒夏特列原理解释,故B符合题意;
C. NH3+H2O ![]() NH3H2O
NH3H2O ![]() NH4++OH-,加入氢氧化钠,增大氢氧根离子浓度,平衡逆向移动,有利于氨气的生成,故能用勒夏特列原理解释,故C不符合;
NH4++OH-,加入氢氧化钠,增大氢氧根离子浓度,平衡逆向移动,有利于氨气的生成,故能用勒夏特列原理解释,故C不符合;
D. 反应![]() 是气体体积减小的反应,增大压强,反应正向移动,有利于SO2和O2反应生成SO3,故能用勒夏特列原理解释,故D不符合;
是气体体积减小的反应,增大压强,反应正向移动,有利于SO2和O2反应生成SO3,故能用勒夏特列原理解释,故D不符合;
故选B。

练习册系列答案
相关题目
【题目】高炉炼铁过程中发生反应:![]() Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g) ![]()
![]() Fe(s)+CO2(g),该反应在不同温度下的平衡常数见表。
Fe(s)+CO2(g),该反应在不同温度下的平衡常数见表。
温度T/℃ | 1000 | 1150 | 1300 |
平衡常数K | 4.0 | 3.7 | 3.5 |
下列说法正确的是
A. 增加高炉的高度可以有效降低炼铁尾气中CO的含量
B. 由表中数据可判断该反应:反应物的总能量>生成物的总能量
C. 为了使该反应的K增大,可以在其他条件不变时,增大c(CO)
D. 1000℃下Fe2O3与CO反应,t min达到平衡时c(CO) =2×10-3 mol/L,则用CO表示该反应的平均速率为![]() mol/(L·min)
mol/(L·min)