题目内容
在密闭容器中进行的如下反应:?2SO2(g)+O2(g)![]() 2SO3(g)?
2SO3(g)?
SO2的起始浓度是0.4 mol·L-1,O2的起始浓度是1 mol·L-1。当SO2的转化率为80%时,反应达到平衡状态。
(1)求反应的平衡常数。?
(2)若将平衡时反应混合物的压强增大1倍,平衡将如何移动??
(3)若平衡时反应混合物的压强减小1倍,平衡将如何移动??
(4)平衡时保持体积不变,向平衡混合气体中充入稀有气体Ar,使体系总压变为原来的3倍,平衡又将如何移动???????????
解析:
2SO2(g) + O2(g) ![]() 2SO3(g)?
2SO3(g)?
2 1 2?
起始时 0.4 1 0?
平衡时 0.4×(1-80%)=0.08 1-![]() ×0.4×80%=0.84 0.4×80%=0.32?
×0.4×80%=0.84 0.4×80%=0.32?
(1)平衡常数K=![]() ≈19。?
≈19。?
(2)压强增大1倍,各组分的浓度增大1倍,?
Q=![]() 。?
。?
即Q<K,所以平衡向正反应方向移动。?
(3)压强减小1倍,各组分的浓度也减小1倍。?
Q=![]() 。?
。?
即Qc>K,所以平衡向逆反应方向移动。?
(4)保持体积不变,充入稀有气体Ar,尽管总压改变,但反应混合物各组分的浓度保持不变。?
Q=![]() =K,所以平衡不发生移动。?
=K,所以平衡不发生移动。?
答案:(1)K≈19?
(2)向正反应方向移动?
(3)向逆反应方向移动?
(4)平衡不移动?

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
 已知某可逆反应:mA(g)+nB(g)?pC(g)△H=Q kJ?mol-1,在密闭容器中进行,如图表示在不同时间t、温度T、压强P与反应物B的百分含量的关系曲线,下列判断正确的是( )
已知某可逆反应:mA(g)+nB(g)?pC(g)△H=Q kJ?mol-1,在密闭容器中进行,如图表示在不同时间t、温度T、压强P与反应物B的百分含量的关系曲线,下列判断正确的是( )| A、T2>T1?P1>P2 m+n>p??△Η<0 | B、T1>T2?P1<P2 m+n<p??△Η>0 | C、T1<T2?P1<P2 m+n<p??△Η<0 | D、T1>T2?P1<P2 m+n>p??△Η>0 |
 qC(g)在密闭容器中进行.如图所示反应在不同时间t,温度T和压强P与反应物B的体积分数的关系曲线.根据图象填空((1)、(2)、(3)题填“>”、“<”或“=”):
qC(g)在密闭容器中进行.如图所示反应在不同时间t,温度T和压强P与反应物B的体积分数的关系曲线.根据图象填空((1)、(2)、(3)题填“>”、“<”或“=”):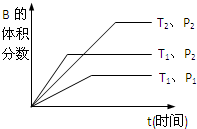
 已知某可逆反应mA(g)+nB(g)?qC(g)在密闭容器中进行.如图所示反应在不同时间t,温度T和压强P与反应物B的体积分数的关系曲线.根据图象填空(填“>”、“<”或“=”):(1)温度的关系:T1
已知某可逆反应mA(g)+nB(g)?qC(g)在密闭容器中进行.如图所示反应在不同时间t,温度T和压强P与反应物B的体积分数的关系曲线.根据图象填空(填“>”、“<”或“=”):(1)温度的关系:T1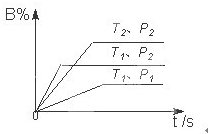 已知某可逆反应m A(g)+n B(g)?p C(g)△H,在密闭容器中进行,如图表示在不同反应时间t 时温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线.由曲线分析,下列判断正确的是( )
已知某可逆反应m A(g)+n B(g)?p C(g)△H,在密闭容器中进行,如图表示在不同反应时间t 时温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线.由曲线分析,下列判断正确的是( ) 已知某可逆反应mA(g)+nB(g)?pC(g),在密闭容器中进行,如图表示在不同反应时间t、温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析,下列判断正确的是( )
已知某可逆反应mA(g)+nB(g)?pC(g),在密闭容器中进行,如图表示在不同反应时间t、温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析,下列判断正确的是( )