题目内容
下列叙述正确的是
- A.铁在氯气中燃烧产生浅绿色烟。
- B.钠长期露置于空气中最后生成碳酸钠。
- C.强电解质溶液的导电能力一定比弱电解质溶液的导电能力强。
- D.胶体中分散质能透过半透膜,但不能透过滤纸。
B
试题分析:A不正确,铁在氯气中燃烧生成的是氯化铁,产生棕黄色的烟;溶液的导电性和溶液中离子浓度大小以及离子所带电荷数多少有关系,而与电解质的强弱无关,C不正确;胶体不能透过半透膜,但可以透过滤纸,D不正确,答案选B。
考点:考查物质的性质、溶液的导电性以及胶体的性质等
点评:本题容易错选C。所以在进行溶液导电性判断时,应该具体问题具体分析,而不能只看表象,特别要注意知识的灵活运用。
试题分析:A不正确,铁在氯气中燃烧生成的是氯化铁,产生棕黄色的烟;溶液的导电性和溶液中离子浓度大小以及离子所带电荷数多少有关系,而与电解质的强弱无关,C不正确;胶体不能透过半透膜,但可以透过滤纸,D不正确,答案选B。
考点:考查物质的性质、溶液的导电性以及胶体的性质等
点评:本题容易错选C。所以在进行溶液导电性判断时,应该具体问题具体分析,而不能只看表象,特别要注意知识的灵活运用。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
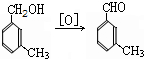
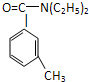 避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH
避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH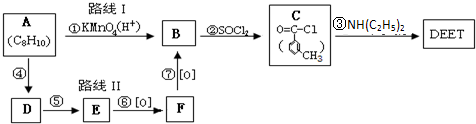
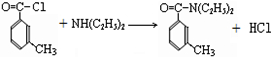
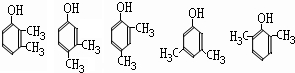 (任写2种)
(任写2种)
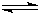 NH3?H2O+H+
NH3?H2O+H+ (2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.
(2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.