题目内容
(08上海重点中学第二次联考)在pH为4~5的环境中,Cu2+、Fe2+不生成沉淀,而Fe3+几乎完全沉淀。工业上制CuCl2是将浓盐酸用蒸
汽加热到80℃左右,再慢慢加入粗氧化铜(含杂质FeO),充分搅拌使之溶解。欲除去溶液中的杂质离子,下述方法正确的是
A . 加入纯Cu将Fe2+还原
B . 向溶液中加入(NH4)2S使Fe2+沉淀
C .直接加水加热使杂质离子水解除去
D .在溶液中通入Cl2,再加入CuO粉末调节pH为4~5
答案;D

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
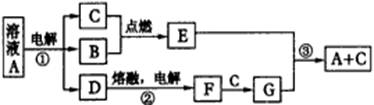
(08上海重点中学第二次联考)A、B、C、D、E、F、G是由短周期元素组成的七种物质,其中B、C、F是单质;常温下B、C、E为气体;A物质的焰色反应呈黄色。(下图中反应②的部分产物未表示出来。)
|
各物质间的转化关系 |
根据上图所示转化关系回答:
(1)经测定G属于离子化合物,其电子式为___________。
(2)写反应②的电极反应式:
阳极___________ ; 阴极___ 。
(3)反应③的化学方程式为___ 。
(4)这七种物质中含有共价键的有___________ (用化学式回答)。