题目内容
(8分)、钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”。试回答下列问题:
(1)钛有 Ti和
Ti和 Ti两种原子,它们互称为 。Ti元素在元素周期表中的位置是第
周期,第 族;按电子排布Ti元素在元素周期表分区中属于
(填s、p、d、ds或f)区元素
Ti两种原子,它们互称为 。Ti元素在元素周期表中的位置是第
周期,第 族;按电子排布Ti元素在元素周期表分区中属于
(填s、p、d、ds或f)区元素
(2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用。偏钛酸钡为离子晶体,晶胞的结构如右图所示,它的化学式是

(3)现有含Ti3+的配合物,化学式为TiCl3(H2O)6,将1mol该物质溶于水,加入足量硝酸银溶液,立即沉淀的氯化银为1mol,已知该配合物的配位数为6,则该配合物的配位体是 。
1mol该配合物外界所含结晶水物质的量为 mol。
(1)同位素 4;IVB族;d (2)BaTiO3 (3)Cl- 和 H2O,1
【解析】(1)质子数相同,中子数不同的同一种元素的不同核素互称为同位素,所以 Ti和
Ti和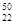 Ti两种原子,它们互称为同位素。Ti的原子序数是22,因此在周期表中的位置是第四最强第ⅣB。由于最后填入的单质是3d电子,所以属于d区。
Ti两种原子,它们互称为同位素。Ti的原子序数是22,因此在周期表中的位置是第四最强第ⅣB。由于最后填入的单质是3d电子,所以属于d区。
(2)根据晶胞的结构示意图可知,Ti原子数8×1/8=1,氧原子数是12×1/4=3个,钡在中心,全部属于该晶胞,属于其化学式为BaTiO3。
(3)由于只能产生1mol氯化银沉淀,所以作为配体的氯离子是2个。因为配位数是6,所以作为配体的水是4个。所以含有的结晶水是2mol。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案(12分)
(1)五种元素的原子电子层结构如下:A:1s22s22p63s2 B:1s22s22p63s23p63d54s2 C:1s22s1 D:1s22s22p63s23p2 E:1s22s22p6。请回答:(填元素符号)
元素的电负性最大, 元素原子的第一电离能最小, 元素最可能生成具有催化性质的氧化物。
(2)钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”, 钛有4822Ti和5022Ti两种原子,它们互称为 。Ti元素在元素周期表中的位置是第 ,按电子排布Ti元素在元素周期表分区中属于 区元素。
(3)A、B两种元素的电离能数据如下(kJ·mol—1):
|
电离能/kJ•mol-1 |
I1 |
I2 |
I3 |
I4 |
|
A |
577 |
1817 |
2745 |
11578 |
|
B |
738 |
1451 |
7733 |
10540 |
化合价是元素的一种性质。由A、B的电离能数据判断,A通常显 价,B显 价。
(4)气态氯化铝(Al2Cl6)是具有配位键的化合物,分子中原子间成键的关系如下图所示。请将图中你认为是配位键的斜线上加上箭头。

(5)假设原子晶体SiO2中Si原子被铝原子取代,不足的价数由钾原子补充。当有25%的硅原子被铝原子取代时,可形成正长石。则正长石的化学组成为 。
(6)CO2与SiO2比较沸点相差很大的原因是 。
 [化学--物质结构与性质
[化学--物质结构与性质  (2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构如右图所示,它的化学式是
(2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构如右图所示,它的化学式是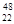 Ti和
Ti和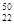 Ti两种原子,它们互称为 。Ti元素在元素周期表中的位置是第 周期,第 族;按电子排布Ti元素在元素周期表分区中属于 (填s、p、d、ds或f)区元素
Ti两种原子,它们互称为 。Ti元素在元素周期表中的位置是第 周期,第 族;按电子排布Ti元素在元素周期表分区中属于 (填s、p、d、ds或f)区元素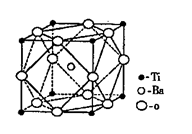
 Ti和
Ti和 Ti两种原子,它们互称为
。Ti元素在元素周期表中的位置是第 周期,第
族;基态原子的电子排布式为
;按电子排布Ti元素在元素周期表分区中属于 区元素
Ti两种原子,它们互称为
。Ti元素在元素周期表中的位置是第 周期,第
族;基态原子的电子排布式为
;按电子排布Ti元素在元素周期表分区中属于 区元素