题目内容
将4.6g钠投入到足量水中,得到a g溶液,将4.8g镁投入到足量盐酸中,得到b g溶液.假设水的质量和盐酸的质量相等,则反应后两溶液质量关系是( )
| A、a=b | B、a>b |
| C、a<b | D、无法判断 |
考点:钠的化学性质,化学方程式的有关计算
专题:几种重要的金属及其化合物
分析:根据 2Na+2H2O=2NaOH+H2↑、Mg+2HCl=2NaCl+H2↑,利用差量法来计算.
解答:
解:设金属钠与水反应生成氢气的质量为x,镁与盐酸反应生成氢气的质量为y,则
2Na+2H2O=2NaOH+H2↑
46 2
4.6g x
=
,解得x=0.2g,
溶液增重4.6g-0.2g=4.4g,
Mg+2HCl=2NaCl+H2↑
24 2
4.8g y
=
,解得y=0.4g,
溶液增重为4.8g-0.4g=4.4g,
所以溶液质量a=b,
故选A.
2Na+2H2O=2NaOH+H2↑
46 2
4.6g x
| 46 |
| 4.6 |
| 2 |
| x |
溶液增重4.6g-0.2g=4.4g,
Mg+2HCl=2NaCl+H2↑
24 2
4.8g y
| 24 |
| 4.8 |
| 2 |
| y |
溶液增重为4.8g-0.4g=4.4g,
所以溶液质量a=b,
故选A.
点评:本题考查了溶液质量的变化,根据物质间的反应来确定溶液增加的量,从而得出结论,难度不大.

练习册系列答案
 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
两种气态烃以一定比例混合,在105℃时1L该混合气体与9L O2混合,充分燃烧后恢复到原状态,所得气体体积仍为10L,下列各组混合烃中,不符合此条件的是( )
| A、CH4 C2H4 |
| B、CH4 C3H6 |
| C、C2H4 C3H4 |
| D、C2H2 C2H6 |
危险化学品的包装标签上要印有警示性标志.下列物质选用如图标志的是( )


| A、汽油 | B、食盐 | C、浓硫酸 | D、炸药 |
维生素E是一种脂溶性维生素,对抗衰老等有特殊作用,经研究发现维生素E有α、β、γ、δ四种类型,其结构简式如图所示(R为-CH2CH2CH2[CH(CH3)CH2CH2]2CH(CH3)2). 上述互为同分异构体的是( )


| A、α β |
| B、β γ |
| C、γδ |
| D、α δ |
决定金属还原性强弱的主要因素是( )
| A、1个金属原子失去电子的多少 |
| B、1摩金属失去电子的多少 |
| C、原子失去电子能力的大小 |
| D、1摩金属与水反应放出H2的多少 |
有关氨气的实验较多,下面对这些实验的实验原理的分析中,正确的是( )
| A、氨气极易溶解于水的性质可以解释氨气的喷泉实验 |
| B、氨气的还原性可以解释氨气与氯化氢的反应 |
| C、铵盐的水溶性大是实验室中用NH4Cl和Ca(OH)2的混合物制取氨气的原因 |
| D、实验室可以用浓硫酸来干燥氨气 |
下列反应属于吸热反应的是( )
| A、铜与硫蒸气反应 |
| B、Mg粉与水反应 |
| C、干冰升华为气体 |
| D、硫酸钙高温锻烧 |
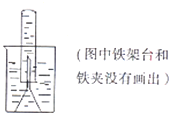 某同学取一张铝箔,并用针刺一些小孔,然后取一药匙过氧化钠粉末,用铝箔包好,放入如图所示装置倒扣的漏斗中.
某同学取一张铝箔,并用针刺一些小孔,然后取一药匙过氧化钠粉末,用铝箔包好,放入如图所示装置倒扣的漏斗中. )是其中的一种,它可以从茉莉花中提取.一种合成路线如下:
)是其中的一种,它可以从茉莉花中提取.一种合成路线如下: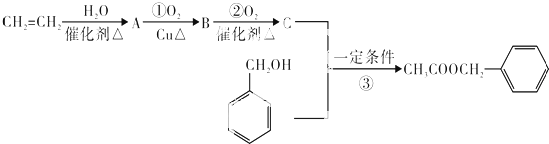
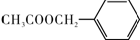 )的说法正确的是
)的说法正确的是