题目内容
 右图所示装置I是一种可充电电池,装置II为电解池。离子交换膜只允许Na
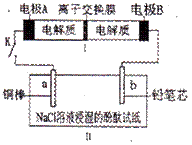
右图所示装置I是一种可充电电池,装置II为电解池。离子交换膜只允许Na![]() 通过,充 放电的化学方程式为2Na2S2+NaBr3 Na2S4+3NaBr。闭合开关K时,b极附近先变红色。下列说法正确的是
通过,充 放电的化学方程式为2Na2S2+NaBr3 Na2S4+3NaBr。闭合开关K时,b极附近先变红色。下列说法正确的是
A.负极反应为4Na![]() 4e
4e![]() =
=![]() 4Na
4Na![]()
B.当有0.01 mol Na![]() 通过离子交换膜时,b电极上析出标准状况下的气体
通过离子交换膜时,b电极上析出标准状况下的气体![]() 112 mL
112 mL
C.闭合K后,b电极附近的pH变小
D.闭合K后,a电极上有气体产生
【错误分析】错选C或D,错选C认为b极发生了
2Cl--2e- ===Cl2↑,Cl2+ H2O=HCl+HClO,错选D是认为a 极发生了2H2O-2e- ===H2↑+
2OH-。对于电解饱和食盐水原理不清析,阳极电极反应式为:2Cl--2e- ===Cl2↑,阴极电极反应式为:2H2O-4e- ===H2↑+2OH-,活波金属与电源正极相连首先失去电子。
【答案】B
【状元纠错】本题信息新颖,多数同学被所给的电池反应很不熟悉,习惯写出电极式的同学会因为写不出电极反应式而做不出来。电源的正极:Br3-+2 e-=3Br- 电源的负极2 S22--2 e-= S42-,内电路为Na+移动导电。由题意可知b极(阴极):2H2O-2e- ===H2↑+2OH-,a 极(阳极):Cu-2 e-= Cu2+,所以C,D均错误。对于B项当有0.01 mol Na![]() 通过离子交换膜时,说明有内电路通过了0.01 mol的电荷,外电路转移的电子也就为0.01 mol。结合b极反应,产生的气体就为0.005 mol,体积为112 mL。只有B正确。
通过离子交换膜时,说明有内电路通过了0.01 mol的电荷,外电路转移的电子也就为0.01 mol。结合b极反应,产生的气体就为0.005 mol,体积为112 mL。只有B正确。

下列为元素周期表的一部分,表中阿拉伯数字(1、2……)是原周期表中行或列的序号。请参照元素A~I在表中的位置,回答下列问题。

(1)B、C两元素中非金属性较强的是 (写出元素名称),请设计一个简单的实验证明这一结论 。
(2)表中某元素能形成两性氧化物,写出该氧化物溶于氢氧化钠溶液的离子反应方程式
(3)表中某元素的单质在常温下为气态,该元素能与A~I中的一种元素构成原子个数比为1:1和1:2的两种共价化合物X和Y,该元素还能与A~I中的另一种元素构成离子个数比为1:1和1:2的两种离子化合物Z和M。写出Z与Y反应的化学方程式: 。
|
实验室中采用右图所示装置模拟工业上同时制取元素A和I
的单质过程:
①写出电极C1上发生反应的电极反应式 。
②当电极上产生112mL(标准状况)元素I单质气体时(假设
气体完全逸出,溶液体积不变),烧杯中溶液的pH= 。
(![]() )
)
下列为元素周期表的一部分,表中阿拉伯数字(1、2……)是原周期表中行或列的序号。请参照元素A~I在表中的位置,回答下列问题。
(1)B、C两元素中非金属性较强的是 (写出元素名称),请设计一个简单的实验证明这一结论 。
(2)表中某元素能形成两性氧化物,写出该氧化物溶于氢氧化钠溶液的离子反应方程式
(3)表中某元素的单质在常温下为气态,该元素能与A~I中的一种元素构成原子个数比为1:1和1:2的两种共价化合物X和Y,该元素还能与A~I中的另一种元素构成离子个数比为1:1和1:2的两种离子化合物Z和M。写出Z与Y反应的化学方程式: 。
|
的单质过程:
①写出电极C1上发生反应的电极反应式 。
②当电极上产生112mL(标准状况)元素I单质气体时(假设
气体完全逸出,溶液体积不变),烧杯中溶液的pH= 。
(
 )
) 

 ② Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物。请回答:
② Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物。请回答: